Achte Reihe von Experimental-Untersuchungen über Elektricität
[Uebersandt vom Hrn. Verfasser in einem besonderen Abzuge aus den Philosoph. Transact. f. 1834, pt. II. – Die siebente Reihe findet sich in diesen Annal. Bd. XXXIII S. 301, 433, 481, die sechste Reihe nebst dem Nachweis zu den früheren Reihen in demselben Bande, S. 149.]
875) Die große Frage über den Ursprung der Elektricität in der voltaschen Säule hat so viele ausgezeichnete Physiker beschäftigt, daß ein Unbefangener, welcher zwar diese Aufgabe nicht studirt hätte, aber doch die Talente dieser Männer zu würdigen verstände, glauben könnte, die Wahrheit wäre hier einigermaßen aufgedeckt. Wenn aber derselbe in diesem Glauben eine Vergleichung der Resultate und Schlüsse unternähme, würde er bald auf solche Widersprüche gerathen, auf solches Gleichgewicht der Meinung, solche Variation und Combination der Theorie, daß er völlig in Zweifel bleiben müßte, was er für die wahre Auslegung der Natur zu halten habe. Er würde genöthigt seyn, die Versuche zu wiederholen, und dann statt des Urtheils Anderer sein eigenes zu gebrauchen.
876) Diese Sachlage mag mich in den Augen Derer, die bereits über diesen Gegenstand nachgedacht haben, entschuldigen, daß ich auf eine Untersuchung desselben [2] eingegangen bin. Meine Ansichten über die feste Wirkung der Elektricität auf die in Zersetzung begriffenen Körper (783) und über die Einerleiheit der dabei angewandten Kraft mit der zu überwältigenden (855), gegründet nicht auf eine bloße Meinung oder oberflächliche Kenntniß, sondern auf ganz neue, meiner Einsicht nach genaue und entscheidende Thatsachen, setzen mich, glaube ich, in den Stand, die Aufgabe unter Vortheilen zu untersuchen, die keiner meiner Vorgänger besaß und mir Ersatz für deren höheren Scharfsinn leisten. Betrachtungen dieser Art haben mich veranlaßt, zu glauben, ich möchte zur Entscheidung der Frage Einiges beitragen können, und im Stande seyn, an dem großen Werke der Entfernung zweifelhafter Kenntnisse mitzuwirken. Solche Kenntnisse bilden das frühe Dämmerungslicht in jeder fortschreitenden Wissenschaft, und sind wesentlich für deren Entwicklung; allein der, welcher sich bemüht, das Trügerische in derselben zu zerstreuen und das Wahre deutlicher an’s Licht zu ziehen, ist eben so nützlich an seinem Platz und eben so nothwendig in dem Fortgang der Wissenschaft als der, welcher zuerst in die intellectuelle Finsterniß einbricht und zuvor unbekannte Bahnen zur Erkenntniß aufschließt.
877) Die Einerleiheit der Kraft, welche den voltaschen Strom oder das elektrische Agens ausmacht, mit derjenigen, welche die Elemente elektrolytisch zusammenhält (855), oder in anderen Worten, mit der chemischen Verwandtschaft, schien darauf hinzudeuten, daß die Elektricität der Säule nichts anderes sey als eine Aeußerungs-, Erscheinungs- oder Daseynsweise der wahren chemischen Action oder vielmehr ihrer Ursache; und ich habe demgemäß bereits gesagt, daß ich mit Denen übereinstimme, welche glauben, daß die Elektricität von chemischen Kräften hergegeben werde (857).
878) Allein die große Frage, ob sie ursprünglich von dem Metallcontact oder der chemischen Action herrühre, [3] d. h. ob jener oder diese den Strom erzeuge und bedinge, war mir noch zweifelhaft; und der schöne und einfache Versuch mit Platin und amalgamirtem Zink, welchen ich, nebst den Resultaten, umständlich beschrieben habe (863 u. ff.), entscheidet diesen Punkt nicht; denn in jenem Versuch findet die chemische Action nicht ohne Berührung der Metalle statt, und der Metallcontact ist unwirksam ohne die chemische Action. Mithin kann jener wie diese als die bedingende Ursache des Stroms angesehen werden.
879) Ich hielt es für nothwendig, diese Frage durch die möglichst einfachsten Formen des Apparats und des Versuchs zu entscheiden, damit kein Trugschluß sich unversehens einschleiche. Die bekannte Schwierigkeit, Zersetzungen durch ein einfaches Plattenpaar hervorzubringen, es sey denn in der diese Platten zur Thätigkeit anregenden Flüssigkeit selbst (863), schien mir bei dergleichen Versuchen ein unübersteigliches Hinderniß in den Weg zu legen; allein ich erinnerte mich der leichten Zersetzbarkeit einer Jodkaliumlösung (316), und da ich keinen theoretischen Grund einsah, warum, wenn Metallcontact unwesentlich sey, nicht ohne denselben eine elektrochemische Zersetzung erhalten werden sollte, ging ich an einen solchen Versuch, und zwar mit Erfolg.
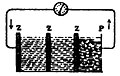
880) Eine Zinkplatte, etwa 8'' lang und 0'',5 breit, wurde gereinigt und in der Mitte rechtwinklich gebogen , Fig. 1 Taf. I. Eine Platinplatte, etwa 3'' lang und 0'',5 breit, wurde an einem Platindraht befestigt und letzterer wie in der Figur gebogen. Beide Metalle wurden wie in der Zeichnung zusammengestellt, allein noch außerhalb des Gefäßes und seines Inhalts, welcher aus verdünnter, mit etwas Salpetersäure gemengter Schwefelsäure bestand. Bei wurde ein zusammengeschlagenes und mit Jodkalium-Lösung befeuchtetes Stück Fließpapier auf das Zink gelegt, und das Ende des Platins darauf gedrückt. Wenn alsdann die Platten in die Säure [4] des Gefäßes getaucht wurden, trat bei sogleich eine Wirkung ein; das Jodid wurde zersetzt, und das Jod erschien an der Anode (663), d. h. an dem Ende des Platindrahts.
881) So lange die Enden der Platten in der Säure blieben, beharrten der elektrische Strom und die Zersetzung bei . Bei Fortrückung des Drahtendes von Stelle zu Stelle auf dem Papier war die Wirkung offenbar sehr kräftig; und als ich ein Stück Kurkumäpapier zwischen das weiße Papier und das Zink legte (beide Papiere mit Jodkalium-Lösung befeuchtet) wurde Alkali an der Kathode (663), d. h. am Zink entwickelt, im Verhältniß zur Jodentwicklung an der Anode. Mithin war die Zersetzung vollkommen polar und entschieden abhängig von einem elektrischen Strom, der vom Zink durch die Säure zum Platin im Gefäße und vom Platin zurück durch die Lösung zum Zink am Papiere ging.
882) Daß die Zersetzung bei eine wahre elektrolytische Action war, herrührend von einem durch die Umstände in dem Gefäße erzeugten Strom, und nicht von einer bloßen directen chemischen Action des Zinks und Platins auf das Jodid, und selbst nicht von einem etwa durch Wirkung der Jodidlösung auf die Metalle bei hervorgerufenen Strom, zeigte sich zunächst durch Herausziehen der Platten aus der Säure in dem Gefäße , wobei alle Zersetzung bei aufhörte, und dann indem man die Metalle entweder in oder außer der Säure in Berührung setzte, wobei zwar eine Zersetzung des Jodids bei eintrat, aber in umgekehrter Ordnung; denn nun erschien das Alkali am Ende des Platindrahts und das Jod am Zink, der Strom ging also gegen vorhin in umgekehrter Richtung und ward erzeugt durch den Unterschied der Wirkung der im Papier enthaltenen Lösung auf die beiden Metalle. Daher verband sich dann das Jod mit dem Zink.
[5] 883) Bei Anstellung dieses Versuchs mit Zinkplatten, die auf ihrer ganzen Oberfläche amalgamirt waren (863), wurden die Resultate mit gleicher Leichtigkeit und in gleichem Sinne erhalten, selbst wenn das Gefäß (Fig. 1 Taf. I) nur verdünnte Schwefelsäure enthielt. Was für ein Ende des Zinks auch in die Säure getaucht war, so blieben doch die Wirkungen sich gleich, so daß, wenn man auch annehmen wollte, das Quecksilber hätte hiebei den Metallcontact abgegeben, doch die Umkehrung des amalgamirten Stücks diesen Einwurf vernichtet haben würde. Der Gebrauch von unamalgamirtem Zink (880) entfernt übrigens jede Möglichkeit eines Zweifels.
884) Als in Verfolgung anderer Ansichten (930) das Gefäß statt der Säure mit einer Lösung von Aetzkali gefüllt wurde, ergaben sich die nämlichen Resultate. Ungehindert trat die Zersetzung des Jodids ein, wiewohl kein Metallcontact von ungleichen Metallen stattfand, und der elektrische Strom gleiche Richtung hatte wie bei Anwendung von Säure.
885) Selbst eine Kochsalzlösung im Glase brachte alle diese Wirkungen hervor.
886) Ein Galvanometer mit Platindrähten, eingeschaltet in die Bahn des Stroms zwischen der Platinplatte und dem Zersetzungsort , zeigte durch seine Ablenkung Ströme von gleicher Richtung an, wie sie durch die chemische Action nachgewiesen waren.
887) Betrachten wir diese Resultate im Allgemeinen, so führen sie zu sehr wichtigen Folgerungen. Zunächst beweisen sie auf’s Entschiedenste, daß Metallcontact nicht nothwendig ist zur Erzeugung eines voltaschen Stroms, und dann zeigen sie eine höchst ungewöhnliche Beziehung zwischen den chemischen Verwandtschaften der Flüssigkeit, die den Strom erregt, und derjenigen, welche durch diesen Strom zersetzt wird.
888) Um die Betrachtung zu vereinfachen, wollen wir zum Versuch mit amalgamirtem Zink zurückkehren. [6] Das so zubereitete Metall zeigt keine Wirkung, ehe nicht der Strom durchgeht; es führt zugleich keine neue Wirkung herbei, sondern entfernt bloß einen Einfluß, welcher entweder für die Erzeugung oder für die Wirkung des elektrischen Stroms fremdartig ist, und welcher, wenn er zugegen ist, bloß die Resultate verwirrt.
889) Man bringe eine amalgamirte Platinplatte parallel über eine Zinkplatte (Fig. 2 Taf. I) und zwischen dieselben, an einem Ende, einen Tropfen verdünnter Schwefelsäure . Es wird nun an dieser Stelle keine merkliche chemische Wirkung eintreten, bis nicht die Platten irgendwo, wie bei , durch einen Elektricität leitenden Körper verbunden werden. Ist dieser Körper ein Metall oder Kohle von gewisser Beschaffenheit, so geht der Strom über, und, da er durch die Flüssigkeit bei circulirt, erfolgt daselbst Zersetzung.
890) Entfernt man nun die Säure bei und bringt einen Tropfen Jodkalium-Lösung nach (Fig. 3 Taf. I), so hat man dieselbe Reihe von Erscheinungen, ausgenommen, daß wenn bei der Metallcontact vollzogen wird, der Elektricitätsstrom gegen früher eine umgekehrte Richtung hat, wie es durch die Pfeile angedeutet ist, welche die Richtung des Stroms bezeichnen (667).
891) Nun sind beide Lösungen Leiter; allein die Leitung in ihnen ist wesentlich mit einer Zersetzung in constanter Ordnung verknüpft (858), und deshalb ergiebt sich aus dem Auftreten der Elemente an gewissen Orten, in welch einer Richtung der Strom bei Anwendung dieser Lösungen gegangen ist. Ueberdieß finden wir, daß wenn sie an den entgegengesetzten Enden der Platten angewandt werden, wie in den beiden letzten Versuchen (889. 890), und der Metallcontact an den andern Enden vollzogen wird, die Ströme entgegengesetzte Richtungen haben. Wir haben es also offenbar in unserer Macht, die gleichzeitige Wirkung zweier Flüssigkeiten an den entgegengesetzten Enden der Platten einander [7] gegenüber zu stellen, und die eine Flüssigkeit als Leiter für die Entladung des Elektricitätsstroms zu gebrauchen, welchen die andere zu erzeugen trachtet; und in der That brauchen wir sie nur für den Metallcontact zu substituiren und beide Versuche zu Einem zu combiniren (Fig. 4 Taf. I). Unter diesen Umständen findet ein Entgegenwirken der Kräfte statt. Die Flüssigkeit, welche die stärkere chemische Verwandtschaft für das Zink in Thätigkeit setzt (d. h. die verdünnte Säure), überwältigt die Kraft der anderen, und bedingt die Bildung und Richtung des elektrischen Stroms; sie macht nicht nur den Strom durch die schwächere Flüssigkeit gehen, sondern kehrt wirklich die Tendenz um, welche die Elemente der letzteren, falls ihnen nicht so entgegengewirkt würde, zu dem Zink und Platin besitzen, und zwingt sie zu einer entgegengesetzten Richtung als sie geneigt sind einzurücken, damit ihr eigner Strom (der der stärkeren Flüssigkeit) freien Lauf gewinne. Entfernt man die vorwaltende Action bei , indem man daselbst den Metallcontact herstellt, so erlangt die Flüssigkeit bei wiederum ihre Kraft; oder bringt man die Metalle bei nicht zum Contact, sondern schwächt nur die Verwandtschaften der Lösung daselbst, während man zugleich die bei verstärkt, so gewinnen die letzteren das Uebergewicht und die Zersetzungen gehen in umgekehrter Ordnung vor sich.892) Ehe ich aus dieser gegenseitigen Abhängigkeit der chemischen Verwandtschaften zweier getrennten Portionen wirkender Flüssigkeiten (916) eine Schlußfolgerung ziehe, will ich noch umständlicher die verschiedenen Umstände untersuchen, unter welchen die Reaction des zersetzten Körpers auf die Action des den voltaschen Strom erzeugenden Körpers, auch in dem Acte der Zersetzung, sichtbar gemacht wird.
893) Der Nutzen des Metallcontacts bei einfachen Plattenpaaren und die Ursache seines großen Vorzugs [8] vor jeder anderen Art von Contact wird nun sehr einleuchtend. Wenn eine amalgamirte Zinkplatte in verdünnte Schwefelsäure getaucht wird, ist die chemische Verwandtschaft zwischen dem Metall und dar Flüssigkeit nicht stark genug, um auf den Berührungsflächen eine merkliche Wirkung hervorzurufen und durch die Oxydation des Metalls eine Wasserzersetzung zu veranlassen; allein sie ist kräftig genug, um einen Elektricitätszustand (oder die die chemische Verwandtschaft bedingende Kraft) zu erregen, welcher einen Strom erzeugen würde, falls der Weg für diesen gebahnt wäre (916. 956), und dieser Strom würde, unter den Umständen, die für die Wasserzersetzung nöthigen Bedingungen vervollständigen.
894) Das Platin, welches zugleich das Zink und die zu zersetzende Flüssigkeit berührt, öffnet durch seine Gegenwart nun der Elektricität die erforderliche Bahn. Seine directe Communication mit dem Zink ist bei weitem wirksamer als mit demselben Metall irgend eine andere, die, wie in dem schon beschriebenen Versuche (891), mittelst zersetzbarer leitender Körper, oder, in anderen Worten, mittelst Elektrolyte vollzogen wäre, weil die chemischen Affinitäten zwischen solchen Elektrolyten und dem Zink eine umgekehrte Wirkung hervorrufen, die der der verdünnten Schwefelsäure widerstreben würde; wenn nun auch diese Action nur schwach ist, muß doch die Verwandtschaft ihrer (der Elektrolyte) Bestandtheile zu einander überwältigt werden, denn sie (die Elektrolyte) können nicht leiten ohne nicht zersetzt zu werden; diese Zersetzung wirkt erfahrungsgemäß auf die Kräfte zurück, welche in der Säure den Strom zu erregen trachten (904. 910 u. s. w.), und in vielen Fällen heben sie dieselben ganz auf. Wo directer Contact zwischen Zink und Platin stattfindet, werden diese Hemmkräfte nicht in Thätigkeit gesetzt, und deshalb wird dann die Erzeugung und Circulation des elektrischen Stroms, so wie die begleitende Zersetzungswirkung ungemein begünstigt.
[9] 895) Es ist jedoch klar, daß man eine dieser entgegengesetzten Wirkungen fortlassen, und dennoch einen Elektrolyt zur Schließung der Kette zwischen dem getrennt in verdünnte Säure getauchten Zink und Platin anwenden kann. Denn wenn man in Fig. 1 Taf. I das Platin mit der Zinkplatte bei in unmittelbarer Berührung erhält, und das Platin irgendwo, wie, bei , durch eine Jodidlösung unterbricht, so übt diese Lösung, weil sie auf beiden Seiten mit Platin in Berührung steht, keine chemische Verwandtschaft auf dieses Metall oder mindestens auf beiden Seiten eine gleiche aus. Ihr Vermögen, einen Strom von umgekehrter Richtung, wie der durch die Wirkung der Säure im Gefäße bedingte, hervorzurufen, ist also aufgehoben, und es bleibt nur ihr Widerstand gegen die Zersetzung durch die von der verdünnten Schwefelsäure ausgeübten Verwandtschaften zu überwältigen übrig.
896) Dieß sind die Umstände bei einem einfachen Plattenpaar, bei dem Metallcontact stattfindet. In solchen Fällen haben die im Gefäße vorwaltenden Verwandtschaften nur ein Paar entgegenwirkender Verwandtschaften zu überwinden; dagegen sind zwei Paare solcher Verwandtschaften zu besiegen, wenn kein Metallcontact zugelassen ist (894).
897) Es ist für schwierig, ja für unmöglich gehalten, Körper durch den Strom eines einfachen Plattenpaars zu zersetzen, selbst wenn dieß so kräftig wirkt, daß es Metallstäbe zum Rothglühen bringt, wie z. B. der Hare’sche Calorimotor, wenn man ihn die Einrichtung einer einfachen Voltaschen oder der so wirksamen Wollastonschen Kette giebt. Diese Schwierigkeit entspringt gänzlich aus dem Antagonismus der den Strom erzeugenden chemischen Verwandtschaft mit der zu überwältigenden, und hängt durchaus von der relativen Intensität beider ab. Denn wenn die Summe der Kräfte jener ein gewisses Uebergewicht über die Summe der Kräfte dieser besitzt, erlangen die ersteren die Oberherrschaft, [10] bedingen den Strom und überwältigen die letzteren, so daß die Substanz, welche diese letzteren äußert, ihre Bestandtheile, sowohl der Richtung als der Menge nach, in völliger Uebereinstimmung mit dem Laufe derer ausgiebt, die die stärkere Wirkung ausüben.
898) In der Wasserzersetzung hat man im Allgemeinen ein chemisches Prüfmittel für den Durchgang eines elektrischen Stroms gesucht. Allein nun begann ich den Grund des Mißlingens einzusehen, so wie auch den einer lange zuvor von mir beim Jodkalium beobachteten Thatsache (315. 316), der nämlich, daß Körper, nach der Beschaffenheit und Intensität ihrer gewöhnlichen chemischen Verwandtschaften, mit ungleicher Leichtigkeit durch einen gegebenen elektrischen Strom zersetzt werden. Dieser Grund schien mir in ihrer Rückwirkung auf die den Strom zu erregen suchenden Verwandtschaften zu liegen, und ich hielt es für wahrscheinlich, daß es viele Substanzen gäbe, die durch den Strom einer einfachen, in verdünnte Schwefelsäure getauchten Zink-Platin-Kette zersetzt werden könnten, wiewohl das Wasser deren Wirkung widersteht. Ich fand bald, daß dieß der Fall sey, und da die Versuche neue und schöne Beweise von der directen Beziehung und Gegenwirkung der den Elektricitätsstrom erzeugenden und der ihm sich widersetzenden chemischen Verwandtschaften darbieten, so werde ich sie in der Kürze beschreiben.
899) Der Apparat war wie in Fig. 5 Taf. I eingerichtet. Das Gefäß enthielt verdünnte Schwefelsäure; war die Zinkplatte, die Platinplatte; , , waren Platindrähte. Die Zersetzungen geschahen bei , und gewöhnlich war bei ein Galvanometer in den Bogen eingeschaltet; es ist hier nur die Stelle desselben angegeben; der Kreis bei hat keine Beziehung zur Größe des Instruments. Bei waren die Einrichtungen verschieden, je nach der Art der Zersetzung, die daselbst vorgenommen werden sollte. Sollte auf einen flüssigen Tropfen eingewirkt werden, wurden bloß die beiden [11] Drahtenden in denselben eingetaucht; sollte eine in den Poren von Papier enthaltene Flüssigkeit zersetzt werden, wurde einer der Drähte verbunden mit einer Platte, auf welcher das Papier lag, während der andere Draht auf dem Papier ruhte (Fig. 12 Taf. I); zuweilen, wie bei Anwendung von Glaubersalz, lagen auf der Platinplatte zwei Stücke Papier, und eins der Enden von und ruhte auf jedem Stück (Fig. 14). Die Pfeile deuten die Richtung des elektrischen Stromes an (667).
900) Eine Jodkalium-Lösung, die in damit benäßtem Papier an die Unterbrechungsstelle bei gebracht worden, wurde leicht zersetzt. Das Jod entwickelte sich an der Anode und das Alkali an der Kathode.
901) Geschmolzenes Zinnchlorür, zersetzte sich ebenfalls leicht bei , gab Zinnchlorid an der Anode (779) und Zinn an der Kathode.
902) Geschmolzenes Chlorsilber entwickelte Chlor an der Anode und glänzendes metallisches Silber an der Kathode, entweder in Häutchen auf der Oberfläche der Flüssigkeit oder in Krystallen darunter.
903) Mit Schwefelsäure gesäuertes Wasser, verdünnte Salzsäure, Glaubersalzlösung, geschmolzener Salpeter, geschmolzenes Chlor- oder Jodblei wurden durch ein bloß durch Schwefelsäure angeregtes einfaches Plattenpaar nicht zersetzt.
904) Diese Versuche beweisen genugsam, daß ein einfaches Plattenpaar Körper elektrolysiren und in ihre Bestandtheile zerlegen kann. Sie zeigen auch in niedlicher Weise die directe Beziehung und Gegenwirkung der chemischen Verwandtschaften an den beiden Wirkungspunkten. In den Fällen, wo die Summe der widerstrebenden Verwandtschaften bei hinreichend kleiner war als die Summe der thätigen Verwandtschaften bei , fand eine Zersetzung statt; allein in den Fällen wo die erstere Summe größer war, widerstand der Körper der Zersetzung und kein Strom ging über (891).
905) Es ist jedoch klar, daß die Summe der thätigen [12] Verwandtschaften bei erhöht werden kann, wenn man andere Flüssigkeiten als verdünnte Schwefelsäure anwendet; im letzteren Falle ist es, glaube ich, bloß die Verwandtschaft des Zinks zu dem im Wasser bereits mit Wasserstoff verbundenen Sauerstoff, durch deren Aeußerung der Strom erregt wird (919); und wenn die Verwandtschaften so erhöht sind, führen die von mir vorgetragenen Ansichten zu dem Schluß, daß Körper, welche in den vorhergehenden Versuchen widerstanden, zersetzt werden müssen, wegen des vergrößerten Unterschiedes zwischen ihren und den so erhöht thätigen Verwandtschaften. Dieß bestätigte sich folgendermaßen.
906) Zu der Flüssigkeit im Gefäße wurde etwas Salpetersäure gesetzt, um eine Mischung zu erhalten, die ich verdünnte Salpeter-Schwefelsäure nennen werde. Bei Wiederholung der Versuche mit dieser Mischung wurden alle zuvor zerlegten Körper wiederum zersetzt, und zwar viel leichter. Allein überdieß gaben jetzt viele, die zuvor der Elektrolysirung widerstanden, ihre Elemente aus. So gab Glaubersalzlösung, mit der Lackmus- und Kurkumäpapier befeuchtet worden, Säure an der Anode und Alkali an der Kathode; Salzsäure, gefärbt durch Indigo, lieferte Chlor an der Anode und Wasserstoff an der Kathode; Lösung von salpetersaurem Silber gab Silber an der Kathode aus. Ferner zeigten sich geschmolzener Salpeter, geschmolzenes Jodblei, geschmolzenes Chlorblei zersetzbar durch den Strom eines einfachen Plattenpaars, was früher (903) nicht der Fall war.
907) Eine Lösung von essigsaurem Blei wurde anscheinend durch dieß Plattenpaar nicht zersetzt, auch mit Schwefelsäure angesäuertes Wasser schien anfangs nichts auszugeben (973).
908) Die Erhöhung der Intensität des von einer einfachen voltaschen Kette hervorgebrachten Stroms mit der Verstärkung der chemischen Action ist hier genugsam deutlich. Um sie jedoch in ein noch helleres Licht zu [13] setzen und um zu zeigen, daß die Zersetzungswirkung in den letzteren Fällen nicht bloß von der Fähigkeit zur Entwicklung von mehr Elektricität abhänge, wurden Versuche angestellt, bei denen die entwickelte (Elektricitäts-) Menge, ohne Veränderung in der Intensität der erregenden Ursache, vergrößert war. So wurden die Versuche, bei denen verdünnte Schwefelsäure gebraucht war (899), mit Anwendung derselben Säure, aber großer Platten von Zink und Platin wiederholt; allein die Körper, welche vorhin der Zersetzung widerstanden, thaten es auch jetzt. Nun nahm ich Salpeter-Schwefelsäure und tauchte in dieselbe bloße Drähte von Platin und Zink; allein ungeachtet dieser letzteren Abänderung wurden nun die Körper zersetzt, welche früher dem durch die verdünnte Schwefelsäure erregten Strom widerstanden. Salzsäure z. B. konnte durch ein einfaches, in verdünnte Schwefelsäure eingetauchtes Plattenpaar nicht zersetzt werden; Verstärkung der Schwefelsäure oder Vergrößerung des Zinks und Platins erhöhten die Wirksamkeit dieses Plattenpaars nicht; allein als ein wenig Salpetersäure zu der verdünnten Schwefelsäure gesetzt ward, erlangte die entwickelte Elektricität die Kraft, Salzsäure zu zersetzen, Chlor an der Anode und Wasserstoff an der Kathode zu entwickeln; selbst wenn die Metalle als bloße Drähte angewandt wurden. Diese Verstärkungsart der Intensität des elektrischen Stroms schließt die von der Vermehrung der Plattenpaare oder selbst die von der Concentration der Säure abhängige Wirkung aus, und ist daher der Beschaffenheit und Stärke der in Thätigkeit gesetzten chemischen Verwandtschaften zuzuschreiben; sie kann, sowohl ihren Principien nach als in Praxis, als völlig verschieden von jeder anderen Verstärkungsart angesehen werden.
909) Die directe Beziehung, welche so in der einfachen voltaschen Kette zwischen der Intensität des elektrischen
[14] Stroms und der Intensität der an dem Orte, wo das Daseyn und die Richtung des elektrischen Stroms bedingt wird, in Thätigkeit gesetzten chemischen Action experimentell nachgewiesen ist, führt zu dem Schluß, daß man, bei Anwendung geeigneter Körper, wie geschmolzener Chloride, Salze, Lösungen von Säuren etc., welche auf die angewandten Metalle mit verschiedenen Graden von chemischer Kraft einwirken, und auch bei Anwendung von Metallen in Verknüpfung mit Platin oder mit anderen, welche in dem Grade der zwischen ihnen und der erregenden Flüssigkeit oder dem Elektrolyte ausgeübten chemischen Action verschieden sind – in den Stand gesetzt werde, eine Reihe von vergleichungsweise constanten, durch elektrische Ströme von verschiedener Intensität hervorgebrachten Wirkungen zu erhalten, und nach diesen eine Skale zu entwerfen, mittelst welcher durch künftige Untersuchungen die relativen Intensitätsgrade genau festzusetzen seyen.
910) Ich habe bereits über die Zersetzung an der Experimentirstelle die Ansicht aufgestellt, sie sey die directe Folge der an einem anderen Orte ausgeübten Kraft von gleicher Art mit der zu überwältigenden, und sey folglich das Resultat eines Antagonismus von Kräften gleicher Natur (891. 904). Die Kräfte an dem Zersetzungsort haben eine Einwirkung auf die erregenden und bestimmenden Kräfte proportional mit dem, was zur Ueberwältigung ihrer selbst erforderlich ist, und daraus entspringt das sonderbare Resultat eines Widerstandes, durch Zersetzungen, gegen die ursprünglich bedingende Kraft, und folglich auch den Strom. Dieß zeigt sich gut in den Fällen, wo Körper, wie Chlorblei, Jodblei und Wasser durch den von einer einfachen Zink-Platin-Kette in Schwefelsäure erzeugten Strom nicht zersetzt werden (903), obschon es geschieht mittelst eines intensiveren, durch stärkere chemische Kräfte hervorgerufenen [15] Stroms. In dergleichen Fällen geht kein merklicher Theil des Stromes durch (967); die Wirkung ist gehemmt; und ich bin jetzt der Meinung, daß bei dem Leitungsgesetz, welches ich in der vierten Reihe dieser Untersuchungen beschrieben habe (413), die Körper, welche im flüssigen Zustand elektrolysirt wurden, darum in fester Gestalt keine Elektrolysirung mehr erlitten, weil die Anziehungen, welche die Theilchen in Verbindung und in ihrer relativen Lage erhielten, zu mächtig waren für den elektrischen Strom. Die Theilchen blieben also in ihrer Stellung, und da die Zersetzung verhindert war, war es auch der Durchlaß der Elektricität. Wenn man auch eine Batterie von vielen Platten anwendet, wird doch, falls sie nur genau von der Art ist, daß keine fremdartige oder indirecte Wirkung (1000) hinzutreten kann, das Ganze der die Thätigkeit jener Batterie betreffenden Verwandtschaften aufgehoben und aufgewogen.
911) In Bezug auf den Widerstand in einzelnen Zersetzungsfällen erhellt indeß, daß, da diese an Stärke verschieden sind, je nach den Verwandtschaften, durch welche die Elemente der Substanz ihre Orte zu behalten streben, sie auch Fälle liefern werden, die eine Reihe von Graden ausmachen, durch welche die ursprünglichen Intensitäten einfacher voltascher oder anderer Elektricitätsströme gemessen werden können, und welche, verbunden mit der durch die verschiedenen Grade der wirkenden Kraft bestimmten Intensitätsskale (909), wahrscheinlich eine hinreichende Reihe von Unterschieden darbieten werden, um fast jedem wichtigen Fall, wo eine Bezugnahme auf die Intensität erforderlich wäre, zu begegnen.
912) Nach den Versuchen, welche ich bisher habe anstellen können, finde ich, daß die folgenden Körper elektrolytisch sind in nachstehender Ordnung, worin jeder durch einen schwächeren Strom zersetzt wird als der [16] nächstfolgende. Diese Ströme waren immer die eines einfachen Plattenpaars, und können als elementare voltasche Ströme angesehen werden.
- Jodkalium (gelöst)
- Chlorsilber (geschmolzen)
- Zinnchlorür (geschmolzen)
- Chlorblei (geschmolzen)
- Jodblei (geschmolzen)
- Salzsäure (gelöst)
- Wasser, gesäuert durch Schwefelsäure.
913) Bei allen Bemühungen, die zur Zersetzung verschiedener Körper erforderliche relative elektrolytische Intensität zu bestimmen, ist es wesentlich, daß man die Natur der Elektrode und der anderen anwesenden Körper, welche secundäre Actionen begünstigen könnten (986) beachte. Wenn bei einer Elektro-Zersetzung eins der abgeschiedenen Elemente eine Verwandtschaft zu der Elektrode oder zu den in der umgebenden Flüssigkeit befindlichen Körpern besitzt, so wird dadurch die der Zersetzung widerstrebende Verwandtschaft zum Theil aufgewogen, und man findet nicht den wahren Ort des Elektrolyts in einer Tafel der obigen Art. So verbindet sich Chlor mit der positiven Platinelektrode leicht, Jod aber beinahe gar nicht, und daher, glaube ich, steht das Chlorid in der vorhergehenden Tafel oben an[1]. Wenn ferner bei der Wasserzersetzung nicht bloß Schwefelsäure, sondern auch etwas Salpetersäure zugegen ist, so wird das Wasser leichter zersetzt, denn der Wasserstoff an der Kathode wird zuletzt nicht ausgetrieben, sondern findet in der Salpetersäure Sauerstoff, mit dem er sich zu einem secundären Resultat verbinden kann. Auf diese Weise sind die der Zersetzung widerstrebenden Verwandtschaften geschwächt, und die Bestandtheile des Wassers können durch einen Strom von geringerer Intensität getrennt werden.
914) Dieses Princip kann man benutzen, um in der [17] bereits (909. 911) erwähnten Skale der Initial-Intensitäten kleinere Grade, als daselbst vorausgesetzt wurden, zu interpoliren; denn indem man die Kraft eines Stroms von constanter Intensität verbindet mit dem Gebrauch von Elektroden, die zu den aus dem zersetzten Elektrolyt entwickelten Elementen mehr oder weniger Verwandtschaft haben, lassen sich verschiedene intermediäre Grade erhalten.
915) Kehren wir zu der Erörterung über die Herkunft der Elektricität (878 etc.) zurück, so giebt es einen andern Beweis der vollkommensten Art, daß der Metallcontact nichts mit der Erzeugung der Elektricität in der voltaschen Kette zu schaffen habe, und ferner, daß die Elektricität nur eine andere Art der Aeußerung chemischer Kräfte sey. Diesen Beweis giebt die Erzeugung des elektrischen Funkens ehe der Metallcontact vollzogen ist, bloß durch die Wirkung rein und ungemischt chemischer Kräfte. Der Versuch, den ich weiterhin beschreiben werde (956), besteht in der Darstellung eines elektrischen Funkens durch Vollziehung des Contacts zwischen einer Zink- und Kupferplatte, die beide in verdünnte Schwefelsäure eingetaucht sind. Um die Vorrichtung so einfach als möglich zu machen, wurden keine amalgamirten Flächen angewandt, sondern der Contact durch einen Kupferdraht vollzogen, der mit der Kupferplatte verbunden war, und dann mit einer blanken Stelle der Zinkplatte in Berührung gesetzt ward. Nun erschien der elektrische Funke, der also nothwendigerweise übergesprungen seyn mußte, ehe Zink und Kupfer in Berührung kamen. (The electric spark appeared, and it must of necessity have existed and passed before etc.)
916) Um die Grundsätze deutlicher zu machen, welche ich aufzustellen bemüht gewesen bin, will ich sie, nach meiner jetzigen Ansicht, in ihrer einfachsten Form [18] aus einander setzen. Die Elektricität der voltaschen Säule (856 Anmerk.) ist, sowohl ihrem Ursprunge als ihrer Fortdauer nach, nicht abhängig von der gegenseitigen Berührung der Metalle (880. 915). Sie rührt gänzlich von chemischer Wirkung her (882), und ist in ihrer Intensität proportional den zu ihrer Erzeugung beitragenden Verwandtschaften (908), so wie ihrer Menge nach proportional der Menge von Substanz, welche während ihrer Entwicklung chemisch thätig ist (869). Diese feste Erzeugung ist wiederum einer der strengsten Beweise, daß die Elektricität chemischen Ursprungs ist.
917) Wie die Erzeugung der voltaschen Elektricität (volta-electro-generation) ein Fall von chemischer Action ist, so ist auch die Zersetzung durch voltasche Elektricität (volta-electro-decomposition) ein bloßer Fall von dem Uebergewicht einer Gruppe (sel) von kräftigeren chemischen Verwandtschaften über eine andere Gruppe von schwächeren; und wenn man das Beispiel zweier entgegenwirkender Gruppen solcher Kräfte (891) erwägt, und sich ihrer wechselseitigen Beziehung und Abhängigkeit erinnert, scheint es nicht nöthig, in Bezug auf solche Fälle, einen andern Ausdruck als den: chemische Verwandtschaft zu gebrauchen (wiewohl der: Elektricität, sehr passend seyn mag), so wenig es nöthig ist irgend ein neues Agens als mitwirkend zur Erzeugung der Resultate vorauszusetzen; denn wir können annehmen, daß die Kräfte an den beiden Orten der Wirkung durch Vermittlung der Metalle (Fig. 4 Taf. I) in directer Gemeinschaft stehen und gegen einander balancirt werden (891), auf ähnliche Art wie es bei mechanischen Kräften mittelst des Hebels der Fall ist (1031).
918) Alle diese Thatsachen zeigen uns, daß die Kraft, die man gewöhnlich chemische Verwandtschaft nennt, durch Metalle und gewisse Kohlenarten in Distanz mitgetheilt werden kann, daß der elektrische Strom nur eine andere Form der chemischen Verwandtschaftskräfte [19] ist, daß seine Kraft den ihn erzeugenden chemischen Verwandtschaften proportional geht, daß wenn er Mangel an Kraft leidet, ihm durch chemische Kräfte aufgeholfen werden kann, daß der Mangel der ersteren durch ein Aequivalent der letzteren ersetzt wird; daß, mit anderen Worten, die Kräfte, welche man Affinität und Elektricität nennt, eins und dasselbe sind.
919) Prüft und vergleicht man die Umstände bei der Erzeugung der Elektricität in der gewöhnlichen voltaschen Kette, so erhellt, daß die Quelle jenes Agens, darunter immer die Elektricität verstanden, welche circulirt und den Strom in dem voltaschen Apparat vervollständigt, diesem Apparate Kraft und Charakter giebt (947. 996), existirt in der chemischen Action, welche direct stattfindet zwischen dem Metall und dem sich mit diesem verbindenden Körper, und durchaus nicht in der späteren Wirkung der dabei erzeugten Substanz auf die vorhandene Säure[2]. So ist, wenn Zink, Platin und verdünnte Schwefelsäure gebraucht werden, die Vereinigung des Zinks mit dem Sauerstoff des Wassers das Bedingende des Stroms; und wiewohl die Säure wesentlich ist zur Fortschaffung des dabei gebildeten Oxyds, damit eine andere Portion Zink auf eine andere Portion Wasser wirken könne, so bringt sie doch durch Verbindung mit jenem Oxyde keine merkliche Portion des circulirenden Stroms hervor. Denn die Quantität der Elektricität hängt ab von der Quantität des oxydirten Zinks und hat ein festes Verhältniß zu derselben; und die Intensität der Elektricität ist proportional der Verwandtschaft des Zinks zu dem Sauerstoff unter den obwaltenden Umständen, und sie erleidet kaum, wenn überhaupt irgend, eine Abänderung durch den Gebrauch von starker oder schwacher Säure (908).
920) Wenn ferner Zink, Platin und Salzsäure gebraucht werden, scheint die Elektricität von der Verwandtschaft [20] des Zinks zum Chlor abzuhängen, und genau im Verhältniß zu der, in der That zu einander aequivalenten Anzahl der sich verbindenden Zink- und Chlortheilchen in Circulation gesetzt zu werden.
921) Allein, wenn man die Oxydation oder eine andere directe Einwirkung auf das Metall selbst als die Ursache und Quelle des elektrischen Stroms betrachtet, ist es von der äußersten Wichtigkeit zu bemerken, daß der Sauerstoff oder andere Körper sich in einem besonderen Zustand, nämlich in dem Zustand der Verbindung befinden muß, und nicht bloß dieß, sondern, ferner beschränkt, in einem solchen Verbindungszustand und solchem Verhältniß, worin er einen Elektrolyten constituirt (823). Eine Zink- und eine Platinplatte, in Sauerstoffgas mit einander verknüpft, vermögen nicht einen elektrischen Strom zu erzeugen oder als eine voltasche Kette zu wirken, selbst wenn man die Temperatur so steigert, daß das Zink sich bei weitem rascher oxydirt als im Fall das Plattenpaar in verdünnte Schwefelsäure getaucht wäre, denn dieser Sauerstoff macht keinen Theil eines Elektrolyten aus, und kann daher die Kräfte vermittelst Zersetzung oder gar wie die Metalle durch sich selbst nicht weiter leiten. Sollte jemand an den gasigen Zustand Anstoß nehmen, so denke er sich flüssiges Chlor. Dieß erregt, indem es sich mit dem Zink verbindet, keinen Elektricitätsstrom durch die beiden Platten, denn seine Theilchen können nicht die an dem Verbindungspunkt thätige Elektricität zu dem Platin durchleiten. Es ist an sich kein Leiter wie die Metalle, auch ist es kein Elektrolyt, also während der Zersetzung nicht der Leitung fähig, und folglich findet an der Stelle eine bloße chemische Action und kein elektrischer Strom statt[3].
[21] 922) Man könnte auf den ersten Blick vermuthen, ein leitender, aber nicht elektrolytischer, Körper vermöge die dritte Substanz zwischen dem Zink und Platin abzugeben, und wahr ist es, daß es dergleichen giebt, welche fähig sind, eine chemische Wirkung auf die Metalle auszuüben. Sie müssen jedoch aus den Metallen selbst genommen werden, denn außer diesen und der Kohle giebt es keine Substanzen dieser Art. Um diesen Gegenstand durch einen Versuch zu entscheiden, machte ich die folgende Vorrichtung. Von geschmolzenem Zinn brachte ich so viel in eine V-förmig gebogene Röhre, daß deren Arme zur Hälfte gefüllt wurden (Fig. 6 Taf. I) und steckte darauf zwei dicke Platindrähte bis zu einer gewissen Tiefe in das Zinn, ließ nun das Ganze erkalten, und verband die Enden und mit einem empfindlichen Galvanometer. Darauf erhitzte ich bei die Röhre auf’s Neue, während der Arm kalt gelassen wurde. Sogleich wurde das Galvanometer durch den thermoelektrischen Strom ergriffen. Ich steigerte die Hitze bei fortwährend, bis endlich Zinn und Platin sich daselbst verbanden, was bekanntlich unter einer starken chemischen Action und lebhafter Erglühung geschieht; allein dennoch wurde die Wirkung auf das Galvanometer nicht im Mindesten dabei erhöht. Während der ganzen Zeit war keine andere Ablenkung zu beobachten als die von dem thermo-elektrischen Strom herrührende. Wiewohl hier also ein Leiter, und zwar ein chemisch auf das Zinn wirkender, angewandt wurde, ließ sich doch, da derselbe kein Elektrolyt war, nicht die geringste Wirkung eines elektrischen Stroms verspüren (947).
[22] 923) Diesem nach ist es augenscheinlich, daß die Eigenthümlichkeit eines Elektrolyte ein wesentlicher Theil der voltaschen Kette ist; und wenn man die Natur eines Elektrolyten in Betracht zieht, ergeben sich gute Gründe, warum er, und nur er allein, wirksam seyn kann. Ein Elektrolyt ist immer ein zusammengesetzter Körper; er ist leitend, aber nur während er zersetzt wird. Seine Leitung hängt ab von seiner Zersetzung und von der Fortführung seiner Theilchen in parallelen Richtungen mit dem Strom; und so innig ist diese Verknüpfung, daß wenn der Fortführung Einhalt geschieht, auch der Strom gehemmt ist, wenn die Bahn der ersteren verändert wird, die Bahn und Richtung des letzteren ebenfalls geändert werden. Die Theilchen eines elektrolytischen Körpers sind alle so wechselseitig verknüpft, stehen, durch ihre ganze Erstreckung in Richtung des Stroms, in solcher Beziehung zu einander, daß, wenn das letzte nicht abgegeben wird, das erste auch nicht die Freiheit hat, in die neue Verbindung einzugehen, welche die kräftige Verwandtschaft des wirksamsten Metalls zu erzeugen trachtet; und dann ist der Strom selbst gehemmt; denn die Abhängigkeiten des Stroms und der Zersetzung sind so gegenseitig, daß wer von ihnen ursprünglich bedingt seyn mag, d. h. ob die Bewegung der Theilchen oder die Bewegung des Stroms, die eine unveränderlich in Begleitung der anderen erzeugt wird und in Beziehung zu ihr steht.
924) Betrachten wir nun Wasser als den Elektrolyten und auch als den oxydirenden Körper. Die Anziehung des Sauerstoffs zum Zink ist unter diesen Umständen größer als die des Sauerstoffs zum Wasserstoff; allein indem er sich mit dem Zink verbindet, sucht er einen Elektricitätsstrom in gewisser Richtung in Circulation zu setzen. Diese Richtung hängt zusammen (wie durch unzählige Versuche gefunden) mit der Uebertragung des Wasserstoffs vom Zink zum Platin hin, und mit der entgegengesetzten [23] Fortführung von frischem Sauerstoff vom Platin abwärts gegen das Zink, so daß der Strom nur in Einer Linie fortschreiten kann, und während er fortschreitet, mit Erneuerung der Vorgänge auf der Zinkfläche, die anfangs zugleich die Combination und Circulation bedingten, bestehen und sie begünstigen kann. Daher die Fortdauer sowohl der Wirkung daselbst als die des Stroms. Es ergiebt sich mithin als ganz eben so wesentlich, daß ein Elektrolyt in der Kette zugegen sey, damit die Wirkung in einer gewissen constanten Richtung vorwärts geführt werden könne, als daß ein oxydirender oder ein anderer direct auf das Metall zu wirken fähiger Körper daselbst befindlich sey; und es zeigt sich auch als nothwendig, daß beide Umstände in einen zusammenfließen, oder daß der direct auf das Metall chemisch einwirkende Körper eins von den Ionen des angewandten Elektrolyten sey. Mag nun der voltasche Apparat durch die Lösung einer Säure, oder eines Alkalis, oder Sulphurets, oder durch eine geschmolzene Substanz (476) angeregt worden seyn, so ist dieser Körper bisher doch immer, so viel ich weiß, ein Anion (943) gewesen; und ich schließe aus einer Betrachtung über die Principien der elektrischen Action, daß es nothwendig ein Körper dieser Klasse seyn muß.
925) Betrachtet man die Wirkung der in der voltaschen Kette angewandten Schwefelsäure, so findet man, daß sie unzulänglich ist, durch ihre Verbindung mit dem gebildeten Oxyd, irgend eine merkliche Portion der Elektricität des Stroms hervorzubringen, aus dem einfachen Grunde, weil ihr eine der wesentlichsten Bedingungen abgeht. Sie bildet keinen Theil eines Elektrolyten, noch steht sie in Beziehung zu irgend einem in der Lösung anwesenden Körper, welcher eine gegenseitige Ueberführung der Theilchen und die damit verknüpfte Ueberführung der Elektricität erlaubte. Freilich, da die Fläche, an welcher die Säure das durch Wirkung des Wassers [24] gebildete Oxyd auflöst, mit dem metallischen Zink in Berührung steht, so scheint keine Schwierigkeit in der Betrachtung, daß das Oxyd daselbst einen, seiner chemischen Wirkung auf die Säure proportionalen elektrischen Zustand dem ohne Zersetzung leitenden Metall mittheilen könne. Allein an der Seite der Säure ist keine Substanz zur Vervollständigung des Stroms da; das Wasser als Wasser kann ihn nicht leiten, oder wenigstens einen so kleinen Antheil, daß die Wirkung rein zufällig und fast unwahrnehmbar ist (970); und als ein Elektrolyt kann es ihn nicht leiten, weil ein Elektrolyt vermöge der gegenseitigen Beziehung und Wirkung seiner Theilchen leitet, und weil weder eins der Elemente des Wassers noch das Wasser selbst, so weit wir beobachten können, gegen Schwefelsäure ein Ion ist (818)[4].
926) Diese Ansicht von dem secundären Charakter der Schwefelsäure als eines Agens bei der Erzeugung des voltaschen Stroms wird ferner unterstützt durch die Thatsache, daß der erzeugte und durchgelassene Strom direct und genau proportional ist der Menge des zersetzten Wassers und der Menge des oxydirten Zinks (868. 991), und er ist derselbe wie der, welcher zur Zersetzung einer gleichen Menge Wasser erfordert wird. Da also die Wasserzersetzung zeigt, daß sie die Elektricität hergegeben hat, so bleibt keine andere Elektricität zu erklären, oder irgend eine andere Wirkung als die zwischen dem Zink und dem Wasser stattfindende herzuleiten übrig.
927) Der allgemeine Fall (denn er schließt den früheren (924) ein) bei Säuren und Basen läßt sich theoretisch folgendermaßen angeben. Es sey (Fig. 7 Taf. 1) eine trockne Sauerstoffsäure und eine trockne [25] Base, die sich in berühren, und an ihren Enden durch die Platinplatten , und den Platindraht in elektrischer Gemeinschaft steht. Wenn nun auch Säure und Base flüssig wären und bei eine Verbindung stattfände, mit einer so mächtigen Verwandtschaft, daß sie einen elektrischen Strom hervorzurufen vermöchte, so würde der Strom doch nicht in einem bedeutenden Grade circuliren, weil erfahrungsmäßig weder noch ohne Zersetzung leiten können, denn sie sind unter allen Umständen, ausgenommen gegen sehr schwache Ströme (970. 986) entweder Elektrolyte oder sonst Isolatoren. Nun sind die Verwandtschaften bei nicht von der Art, daß sie die Elemente von oder zu trennen suchten, sondern sie haben nur das Bestreben, beide Körper zu einem Ganzen zu vereinigen. Der Wirkungsort ist daher isolirt, die Wirkung selbst local (921. 947) und es kann kein Strom zu Stande kommen.
928) Wenn Säure und Base in Wasser gelöst sind, dann ist es möglich, daß ein kleiner Antheil der von chemischer Wirkung herrührender Elektricität von dem Wasser ohne Zersetzung fortgeleitet werde (966. 984); allein dieser Antheil wird so klein seyn, daß er zu dem, welcher von dem Aequivalenten der chemischen Kraft herrührt, in gar keinem Verhältniß steht; und da er nicht die wesentlichen Principien der voltaschen Säule involvirt, gehört er nicht zu den hier untersuchten Erscheinungen[5].
929) Wenn statt der Sauerstoffsäure eine Wasserstoffsäure, z. B. Salzsäure, genommen wird (927), so [26] sind die Umstände ganz verändert; dann kann ein Strom, entsprungen aus der chemischen Wirkung der Säure auf die Base, möglicherweise stattfinden. Allein nun wirken beide Körper als Elektrolyten denn jeder liefert nur einen Bestandtheil zur gegenseitigen Verbindung, z. B. einer Chlor, der andere Metall; und der Wasserstoff der Säure und der Sauerstoff der Base stehen bereit, mit dem Chlor der Säure und dem Metall der Base in Uebereinstimmung mit dem Strom, und gemäß den allgemeinen bereits ausführlich entwickelten Grundsätzen, zu wandern.
930) Die Ansicht, daß die Oxydation oder eine andere directe chemische Einwirkung auf das Metall die alleinige Ursache des elektrischen Stroms in der gewöhnlichen voltaschen Säule sey, wird unterstützt durch die Vorgänge, welche stattfinden, wenn Lösungen von Alkalien oder Schwefelalkalien (931. 943) statt der verdünnten Schwefelsäure als elektrolytische Leiter angewandt werden. Die bereits (884) erwähnten Versuche ohne Metallcontact und mit alkalischen Lösungen als erregende Flüssigkeiten wurden gerade zur Erläuterung dieses Punkts angestellt.
931) Es wurden nun die Versuche über die Zersetzung der Körper durch ein einfaches Plattenpaar wiederholt (899), jedoch unter Anwendung einer Aetzkalilauge, statt der Schwefelsäure, in dem Gefäße (Fig. 5 Taf. I), und mit Benutzung der Vortheile, die der Metallcontact darbietet (895). Alle Erscheinungen waren den früheren gleich; das Galvanometer wurde abgelenkt; Lösungen von Jodkalium, salpetersaurem Silber, Salzsäure und Glaubersalz wurden bei zersetzt; und die Orte, wo die abgeschiedenen Bestandtheile erschienen, so wie die Ablenkungen des Galvanometers zeigten einen Strom an von gleicher Richtung, wie wenn Säure im Gefäße war, d. h. derselbe ging vom Zink durch die Lösung zum Platin, und zurück durch das Galvanometer und zersetztwerdende Agens zu dem Zink.
[27] 932) Die Aehnlichkeit in der Wirkung der verdünnten Schwefelsäure und der Kalilauge geht indeß noch viel weiter, selbst bis zur Identität sowohl in der Menge als in der Richtung der erzeugten Elektricität. Eine amalgamirte Zinkplatte erleidet für sich in einer Kalilauge keine merkliche Einwirkung; berührt man sie aber in der Lösung mit einer Platinplatte, so wird an der Oberfläche dieser letzteren Wasserstoff entwickelt, und das Zink oxydirt genau wie wenn es in verdünnte Schwefelsäure eingetaucht wäre (863). Demgemäß wiederholte ich den zuvor beschriebenen Versuch mit gewogenen Zinkplatten (864 etc.), gebrauchte aber dabei Kalilauge statt verdünnter Schwefelsäure. Wiewohl eine viel längere Zeit, als bei Anwendung von Säure erfordert wurde, nämlich drei Stunden für die Oxydation von 7,55 Gran Zink, so fand ich doch, daß der an der Platinplatte entwickelte Wasserstoff zu dem an der Zinkoberfläche gebildeten Oxyde aequivalent war. Mithin findet die ganze Schlußfolge, welche auf das frühere Beispiel anwendbar war, auch hier seine Anwendung: der Strom geht in derselben Richtung, und ihre zersetzende Wirkung hat gleichen Grad von Stärke, wie wenn Säure statt des Alkalis angewandt worden wäre (688).
933) Es scheint mir daher der Beweis vollständig, daß die Verbindung der Säure mit dem Oxyd in dem vorhergehenden Versuch nichts mit der Erzeugung des elektrischen Stroms zu schaffen habe; denn derselbe Strom wird erzeugt, wenn statt der Wirkung der Säure die umgekehrte des Alkalis zugegen ist. Ich glaube nicht, daß man für einen Moment annehmen könne, das Alkali wirke chemisch als eine Säure auf das gebildete Oxyd. Im Gegentheil führen unsere allgemeinen chemischen Kenntnisse zu dem Schluß, daß die gewöhnlichen Metalloxyde eher als Säuren denn als Alkalien wirken; und doch würde diese Art von Wirkung im gegenwärtigen Fall einen umgekehrten Strom zu erregen trachten, wenn das [28] Oxyd des erregenden Metalls bei seiner Verbindung mit dem dazu vorhandenen Körper überhaupt einen Strom hervorbrächte. Allein statt irgend einer Verschiedenheit dieser Art war die Richtung der Elektricität constant, und die Menge derselben auch proportional dem zersetzten Wasser oder dem oxydirten Zink. Man hat Gründe zu glauben, daß Säuren und Alkalien, wenn sie mit Metallen in Contact stehen, auf die sie nicht direct einwirken können, doch einen Einfluß auf deren Anziehungen zum Sauerstoff (941) ausüben. Allein alle Wirkungen in den obigen Versuchen beweisen, glaube ich, daß es die nothwendig von der Elektrolysirung des Wassers (921. 923) abhängige und mit ihr verknüpfte Oxydation des Metalles ist, welche den Strom erzeugt; daß die Säure oder das Alkali bloß als Lösemittel wirkt, durch Fortschaffung des oxydirten Zinks anderen Portionen gestattet neues Wasser zu zersetzen und so die Entwicklung oder Bestimmung des Stromes unterhält.
934) Ich änderte nun die Versuche dahin ab, daß ich eine Ammoniaklösung statt der Kalilösung anwandte, und da sie im Zustande der Reinheit ein schlechter Leiter ist, wie das Wasser (554), wurde sie durch Zusatz von schwefelsaurem Ammoniak leitender gemacht. Allein in allen Fällen waren die Wirkungen dieselben wie vorhin; Zersetzungen gleicher Art fanden statt, und der elektrische Strom, welcher dieselben hervorrief, hatte dieselbe Richtung wie in den eben beschriebenen Versuchen.
935) Um die gleiche und ähnliche Wirkung von Säure und Alkali auf eine noch strengere Probe zu stellen, wurden Vorrichtungen wie in Fig. 8 Taf. I gemacht. Das Glasgefäß enthielt verdünnte Schwefelsäure, das andere eine verdünnte Kalilauge, war eine in beide Flüssigkeiten eingetauchte Platinplatte, und waren amalgamirte Zinkplatten, die mit einem empfindlichen Galvanometer in Verbindung standen. Wenn diese gleichzeitig in die beiden Gefäße getaucht wurden, zeigte [29] sich gewöhnlich zuerst eine schwache Wirkung, und zwar zu Gunsten des Alkalis, d. h. der elektrische Strom suchte durch die Gefäße in Richtung des Pfeils zu gehen, also in umgekehrter Richtung, wie sie von der Säure in allein hervorgebracht worden seyn würde. Allein die Wirkung hörte augenblicklich auf und die Wirkung der Platten in den Gefäßen war so gleich, daß, da sie wegen der umgekehrten Stellung der Platten entgegengesetzt war, kein permanenter Strom daraus entsprang.
936) Manchmal nahm ich statt der Platte eine Zinkplatte, und statt den Platten Platinplatten; allein dieß verursachte keinen Unterschied; auch eine Kupferplatte als mittlere Platte angewandt, brachte keine Aenderung hervor.
937) Da die Entgegenstellung der elektromotorischen Plattenpaare andere Resultate erzeugte, als die von dem bloßen Unterschied ihrer unabhängigen Wirkungen herrührenden (1011. 1045), so ersann ich eine andere Form des Apparats, wobei die Wirkung der Säure und des Alkalis noch directer verglichen werden konnte. Ein cylindrisches Glasgefäß, inwendig etwa zwei Zoll tief und einen Zoll im Durchmesser, von wenigstens einen Viertelzoll dicken Wänden, wurde in der Mitte herunter in zwei Hälften zerschnitten (Fig. 9 Taf. I). Ein breiter Messingring, von größerem Durchmesser als das Gefäß, wurde mit einer Schraube versehen und um die beiden Hälften gelegt, so daß wenn man die Schraube fest anzog, diese Hälften zu einem wasserdichten Gefäß gegen einander gedrückt wurden. Fließpapier von verschiedenen Graden der Permeabilität wurde nun in Stücke von solcher Größe zerschnitten, daß es leicht zwischen die gelösten Hälften des Gefäßes eingeschoben werden konnte, und wenn diese darauf wieder dicht zusammen geschraubt wurden, eine poröse Scheidewand in der Mitte des Gefäßes bildete, die zweien Flüssigkeiten zu beiden Seiten derselben keine andere als eine sehr langsame Vermischung [30] gestattete, aber ihnen doch erlaubte ungehindert als Ein Elektrolyt zu wirken. Die beiden so gebildeten Räume will ich die Zellen und nennen (Fig. 10 Taf. I). Dieß Instrument habe ich bei Untersuchung der Beziehungen von Flüssigkeiten und Metallen unter sich und unter einander von sehr allgemeiner Anwendbarkeit gefunden. Verbindet man es noch mit einem Galvanometer, so ist es leicht damit die Beziehung eines Metalls zu zwei Flüssigkeiten, oder zweier Metalle zu einer Flüssigkeit, oder zweier Flüssigkeiten zu zwei Metallen auszumitteln.
938) Verdünnte Schwefelsäure vom specifischen Gewicht 1,25 wurde in die Zelle gegossen und eine starke Lösung von Aetzkali in die Zelle . Sie mischten sich langsam durch das Papier, und zuletzt bildete sich auf dem Papier, zur Seite des Alkalis, eine dicke Kruste von schwefelsaurem Kali. In jede Zelle wurde eine saubere Platinplatte eingesteckt und mit einem empfindlichen Galvanometer verbunden; allein es konnte kein elektrischer Strom beobachtet werden. Also war der Contact der Säure mit der einen Platinplatte und der des Alkalis mit der andern unfähig einen Strom zu erzeugen, und eben so wenig war die Verbindung der Säure mit dem Alkali wirksamer (925).
939) Wurde eine der Platinplatten fortgenommen und durch eine Zinkplatte ersetzt, so entstand, diese mochte amalgamirt seyn oder nicht, ein starker elektrischer Strom. Allein es war gleich, ob das Zink in die Säure, und das Platin in das Alkali getaucht, oder die umgekehrte Anordnung getroffen war: immer ging der elektrische Strom vom Zink durch den Elektrolyten zum Platin, und von da durch das Galvanometer zurück zu dem Zink. Am stärksten schien der Strom zu seyn, wenn das Zink in dem Alkali und das Platin in der Säure befindlich war.
940) Bei diesen Versuchen schien also die Säure [31] kein Uebergewicht über das Alkali zu haben, vielmehr schwächer als dieses zu seyn. Folglich hat man auch keinen Grund zu der Annahme, die Verbindung des gebildeten Oxyds mit der umgebenden Säure habe einen directen Einfluß auf die Hervorbringung der erregten Elektricität; vielmehr scheint diese ganz von der Oxydation des Metalles herzurühren (919).
941) In der That hat das Alkali ein Uebergewicht über die Säure in der Fähigkeit, das Metall in den sogenannten positiven Zustand zu versetzen. Denn wenn Platten von gleichem Metall, z. B. Zink, Zinn, Blei oder Kupfer zugleich in die Säure und das Alkali eingetaucht werden, geht der elektrische Strom von dem Alkali durch die Zelle zur Säure und zurück durch das Galvanometer zum Alkali, wie schon Humphry Davy früher angegeben[6]. Dieser Strom ist so mächtig, daß wenn man amalgamirtes Zink oder Zinn oder Blei anwendet, das Metall in der Säure, sogleich wie es mit dem Metall in dem Alkali verbunden wird, Wasserstoffgas entwickelt, nicht vermöge einer directen Einwirkung der Säure auf sich, denn wenn der Contact unterbrochen wird, hört die Wirkung auf, sondern weil es in Bezug auf das Metall in dem Alkali stark negativ wird.
942) Die Ueberlegenheit des Alkalis geht ferner daraus hervor, daß, wenn man Zink und Zinn, oder Zinn oder Blei anwendet, das in dem Alkali befindliche Metall, was für eins es auch sey, positiv wird, und das in der Säure negativ. Was für ein Metall sich auch im Alkali befinde, so wird es doch oxydirt; das in der Säure dagegen behält seinen Metallglanz, so weit dieß vom elektrischen Strom abhängt.
943) Dasselbe ergiebt sich auch, wenn man Lösungen von Sulphureten anwendet (930), um zu zeigen, daß [32] es die chemische Wirkung des Metalls und eines der Ionen des angewandten Elektrolyten sey, welche alle Elektricität der voltaschen Kette erzeugt. So geht der Strom, wenn Eisen und Kupfer in verdünnte Säuren getaucht werden, von dem Eisen durch die Flüssigkeit zum Kupfer, wie Humphry Davy gezeigt hat[7]; in Kalilauge hat er dieselbe Richtung, aber in einer Lösung von Schwefelkalium geht er umgekehrt. In den beiden ersten Fällen ist es der mit dem Eisen sich verbindende Sauerstoff, in dem letzteren der mit dem Kupfer sich verbindende Schwefel, durch den der elektrische Strom erzeugt wird. Allein diese beiden Ionen existiren als solche in dem gleichzeitig zersetzt werdenden Elektrolyt; und was mehr ist, sie beide sind Anionen, denn sie entlassen die Elektrolyten an ihren Anoden, und wirken gerade wie Chlor, Jod oder irgend ein anderes Anion gewirkt haben würde, welches statt der zuvor die voltasche Kette in Thätigkeit setzenden genommen worden wäre.
944) Der folgende Versuch vervollständigt die Reihe der Beweise über den Ursprung der Elektricität in der voltaschen Säule. Ein flüssiges Amalgam von Kalium, von diesem Metall nicht mehr als ein Hundertel enthaltend, wurde in Wasser gebracht und durch ein Galvanometer mit einer in demselben Wasser befindlichen Platinplatte verbunden. Sogleich ging ein elektrischer Strom von dem Amalgam durch den Elektrolyt zum Platin. Dieser Strom konnte nur durch die Oxydation des Metalls hervorgerufen seyn, denn es war weder eine Säure noch ein Alkali vorhanden, um sich mit ihm zu verbinden oder auf ihn einzuwirken.
945) Ferner brachte ich eine Platin- und eine blanke Bleiplatte in reines Wasser. Sogleich ging ein starker Strom von dem Blei durch die Flüssigkeit zum Platin. Er war sogar so stark, daß er eine Jodkalium-Lösung zersetzte; die, bei Anwendung des schon (880) Fig. 1 [33] beschriebenen Apparat in die Kette gebracht worden war. Hier gab es keine Wirkung von Säure oder Alkali auf das aus dem Blei gebildete Oxyd, welche die Elektricität geliefert haben könnte; diese rührte also bloß von der Oxydation des Metalles her.
946) Es giebt, meiner Meinung nach, in der Elektricitätslehre keinen wichtigeren Punkt, als den Zustand des Metalls und des elektrolytischen Leiters in der einfachen voltaschen Kette vor und in dem Augenblick der ersten Vollziehung des Metallcontacts. Verständen wir ihn recht, würde uns sicher der Schlüssel zu den Gesetzen, nach denen die große Mannigfaltigkeit der directen und zufälligen voltaschen Erregungen vor sich geht, unmittelbar gegeben und viele neue Felder für die Untersuchung geöffnet seyn.
947) Es scheint, daß wir in vielen Fällen von chemischer Verwandtschaft (z. B. dem vom Zink mit dem Sauerstoff des Wassers etc.) bis zu einem gewissen Grade entscheiden können, welche von den beiden Wirkungsweisen der Anziehungskraft ausgeübt werde (996). Bei der einen Weise können wir die Kraft nach außen fortleiten und sie anderswo das Aequivalent ihrer Wirkung ausüben lassen (867. 917); bei der andern wird sie nicht fortgeführt, sondern an dem Orte (ihrer Entstehung) gänzlich ausgeübt. Das erste ist der Fall bei der volta-elektrischen Erregung, das andere bei der gewöhnlichen chemischen Verwandtschaft; allein beide sind chemische Actionen, und stammen von Einer Kraft oder Einem Principe ab.
948) Die allgemeinen Umstände der ersten Wirkungsweise finden sich bei allen voltaschen Strömen; allein in ihrer Vollkommenheit und frei von denen der zweiten Weise nur in einigen Fällen, z. B. wenn Zink [34] und Platin in Kalilauge, oder amalgamirtes Zink und Platin in verdünnte Schwefelsäure getaucht sind.
949) Angenommen, es sey durch die vorhergehenden Versuche und Betrachtungen hinreichend erwiesen, daß, bei Anwendung von Zink, Platin und verdünnter Schwefelsäure, die elektromotorische Wirkung von der Verwandtschaft zwischen dem metallischen Zink und dem Sauerstoff des Wassers abhänge (921. 924), so ist ersichtlich, daß das Metall für sich unter den obigen Umständen nicht Kraft genug hat, den Sauerstoff aufzunehmen und den Wasserstoff aus seiner Verbindung zu treiben; denn in der That, solch eine Wirkung findet nicht statt. Allein es erhellt auch, daß es durch seine Anziehung zu dem Sauerstoff der mit ihm in Berührung stehenden Theilchen so weit zu wirken vermag, um die ähnlichen Kräfte, welche zwischen diesen und den andern Sauerstofftheilchen und den Wasserstofftheilchen des Wassers bereits wirksam sind, in einen eigenthümlichen Zustand von Spannung oder Polarität zu versetzen; und wahrscheinlich auch, um die Kräfte seiner eigenen Theilchen, welche mit dem Wasser in Berührung sind, in einen ähnlichen Zustand überzuführen. So lange dieser Zustand verbleibt, tritt keine fernere Wirkung ein; allein wenn er durch Schließung der Kette erhöht wird, in welcher die in Bezug auf das Zink und den Elektrolyt nach entgegengesetzten Richtungen wirkenden Kräfte einander genau zu neutralisiren vermögen, dann findet zwischen den Sauerstoff- und Wasserstofftheilchen des Wassers zwischen dem Orte der Steigerung und dem Orte der Wirksamkeit des Zinks eine Reihe von Zersetzungen und Wiederzusammensetzungen statt, denn diese dazwischen befindlichen Theile stehen offenbar in inniger Abhängigkeit und Beziehung zu einander. Das Zink bildet eine directe Verbindung mit denjenigen Sauerstofftheilchen, welche unmittelbar vor ihm in getheilter Relation zu ihm und dem Wasserstoff stehen: das Oxyd wird durch die Säure fortgenommen, und [35] dadurch eine frische Berührungsfläche zwischen dem Zink und Wasser hergestellt, um die Wirkung zu erneuen und zu wiederholen.
950) Practisch wird der Spannungszustand am besten erhöht, wenn man das Metall, welches eine schwächere Anziehung zum Sauerstoff hat als das Zink, in verdünnte Schwefelsäure taucht und es auch mit Zink in Berührung setzt. Die Kraft der chemischen Verwandtschaft, welche in den Wassertheilchen durch die vorherrschende Anziehung des Zinks zum Sauerstoff influencirt oder polarisirt worden ist, wird dann in sehr außerordentlicher Weise durch die beiden Metalle fortgeführt, so daß sie längs der Kette wieder eintritt in den elektrolytischen Leiter, welcher sie nicht ohne Zersetzung, wie es die Metalle thun, fortleiten oder überführen kann; oder wahrscheinlicher wird sie dann durch die Kraft, die gleichzeitig die Verbindung des Zinks mit dem Sauerstoff des Wassers vervollständigt, genau balancirt und neutralisirt. In der That sind die Kräfte der beiden Theilchen, die gegen einander wirken, und folglich entgegengesetzte Richtung haben, die Quelle zweier entgegengesetzten Kräfte oder Kraftrichtungen in dem Strom. Sie sind nothwendig zu einander aequivalent. Da sie in entgegengesetzter Richtung fortgeführt werden, so erzeugen sie den sogenannten Strom; und es scheint mir unmöglich, der Idee zu widerstehen, diesem Strome müsse in der Flüssigkeit und zwischen der Flüssigkeit und dem Zink ein Zustand der Spannung vorausgegangen seyn; die erste Folge der Affinität des Zinks zum Sauerstoff des Wassers.
951) Ich habe mich sorgfältig bemüht, einen Spannungszustand in dem elektrolytischen Leiter aufzufinden; und in der Meinung, daß er entweder vor oder nach der Entladung etwas einer Structur Aehnliches erzeugen möge, gesucht, dasselbe durch polarisirtes Licht sichtbar zu machen. Für eine Glasplatte, 7'' lang, 1½'' breit und 6'' tief, richtete ich zwei Paare Platinelektrode vor, ein Paar [36] für deren Enden und das andere für deren Seiten. Die für die Seiten waren 7'' lang und 3'' hoch, und wurden in der Zelle durch einen mit Kattun überzogenen Holzrahm von einander gehalten, so daß, wenn sie durch Verbindung mit einer Batterie zur Wirksamkeit auf die in die Zelle gegossene Flüssigkeit angeregt worden, die alsdann aufsteigenden Gasblasen den mittleren Theil der Flüssigkeit nicht trüben konnten.
952) Ich goß eine concentrirte Auflösung von schwefelsaurem Natron in die Zelle und verband die Elektroden mit einer Batterie von 150 Paaren vierzölliger Platten. Der Strom ging so ungehindert durch die Zelle, daß die Entladung eben so gut war wie bei Anwendung eines Drahts. Es wurde nun quer gegen die Bahn des elektrischen Stroms ein polarisirter Lichtstrahl durch die Flüssigkeit geleitet und mittelst einer Zerlegungsplatte untersucht. Allein, wiewohl er von der, der Einwirkung der Elektricität unterworfenen Lösung eine sieben Zoll dicke Schicht durchdrungen hatte, und wiewohl der Metallcontact während der Beobachtung bald vollzogen, bald aufgehoben und bald im umgekehrten Sinne hergestellt wurde, war doch nicht die mindeste Spur einer Einwirkung auf den Strahl wahrzunehmen.
953) Nun wurden die großen Elektrode fortgenommen, und die kleineren, für die Enden der Zelle eingerichteten, eingesetzt. In jede derselben war ein Schlitz eingeschnitten, damit man hindurchsehen konnte. Die Bahn des polarisirten Strahls war nun dem Strom parallel oder in Richtung von dessen Axe (517); allein dennoch konnte weder bei Schließung noch bei Oeffnung der Kette irgend eine Wirkung wahrgenommen werden.
954) Bei Anwendung einer starken Lösung von salpetersaurem Blei statt des schwefelsauren Natrons waren die Resultate eben so negativ.
955) Da ich es für möglich hielt, daß die durch die successiven Zersetzungen und Wiederzusammensetzungen [37] des Elektrolyten geschehene Entladung der elektrischen Kräfte jede etwaige Wirkung des anfänglichen Spannungszustandes neutralisirt und deshalb zerstört haben möchten, so nahm ich eine Substanz, die im flüssigen Zustand ein vortrefflicher Elektrolyt, im festen aber ein Isolator ist, nämlich borsaures Blei, in Form einer glasigen Platte, und verband die Seiten und die Ränder dieser Masse mit den Metallplatten und letztere bald mit den Polen einer voltaschen Batterie, bald, um eine Elektricität von höherer Intensität anzuwenden, mit einer Elektrisirmaschine, und leitete nun einen polarisirten Strom bald in dieser, bald in jener Richtung durch die Masse; allein auch jetzt konnte ich nicht die geringste Anzeige von einer Wirkung auf das Licht beobachten. Hieraus schließe ich, daß die Elektrolyte, ungeachtet des neuen und ungewöhnlichen Zustands, welchen sie entweder während der Zersetzung (wo offenbar eine ungeheure Menge Elektricität durch sie geht) annehmen müssen, oder in dem Spannungszustand, welchen sie vorausgesetztermaßen vor der Zersetzung oder in starrer Gestalt besitzen, nicht die Fähigkeit haben auf einen polarisirten Lichtstrahl einzuwirken, da auf keine Weise eine Art von Structur oder Tension in ihnen sichtbar gemacht werden kann.
956) Es giebt jedoch einen schönen experimentellen Beweis, daß die Metalle und die Elektrolyte vor der Erzeugung des elektrischen Stroms und ehe die heterogenen Metalle in Berührung gesetzt werden (915) einen Spannungszustand annehmen. Ich nahm einen voltaschen Apparat, bestehend aus einem Cylinder von amalgamirtem Zink und einem doppelten Cylinder von Kupfer. Diese stellte ich in eine Flasche mit verdünnter Schwefelsäure[8], wo sie nach Belieben durch einen Kupferdraht, der zur Eintauchung in zwei an den Platten befestigten [38] Näpfchen mit Quecksilber vorgerichtet war, in Berührung gesetzt werden konnten.
957) Bei dieser Vorrichtung fand keine chemische Wirkung statt, so lange nicht die Platten in Verbindung gesetzt waren. Allein bei Vollziehung des Contacts kam ein Funke zum Vorschein[9], und die Lösung wurde sogleich zersetzt. Bei Aufhebung des Contacts wurde wieder der gewöhnliche Funke erhalten und die Zersetzung hörte auf. Klar ist, daß hier der Funke vor der Vollziehung des Metallcontacts entstanden seyn muß, denn er ging durch eine Luftschicht, und eben so muß er vor der elektrolytischen Wirkung übergesprungen seyn, denn diese konnte nicht eintreten, ehe nicht der Strom überging, und der Strom konnte nicht übergeben, ehe nicht der Funke erschien. Hiedurch, glaube ich, ist es genugsam bewiesen, daß, so wie das Zink und das Wasser durch ihre gegenseitige Einwirkung die Elektricität des Apparats erzeugen, sie auch durch ihre erste gegenseitige Berührung in einen kräftigen Spannungszustand versetzt werden (951), welcher, obschon nicht fähig eine wirkliche Zersetzung des Wassers zu verursachen, doch im Stande ist, einen elektrischen Funken zwischen dem Zink und einem geeigneten Entlader überspringen zu machen, sobald der Abstand dazu klein genug ist. Der Versuch beweist die directe Erzeugung eines elektrischen Funkens durch rein chemische Kräfte.
958) Mit der Hervorbringung dieses Funkens durch ein einzelnes Plattenpaar sind jedoch einige Umstände verknüpft, die man kennen muß, wenn der Versuch gelingen soll. Wenn die amalgamirten Berührungsflächen ganz [39] blank und trocken sind, ist der Funke bei Vollziehung des Contacts eben so glänzend, wo nicht glänzender als bei Aufhebung desselben. Befindet sich dagegen auf der Quecksilberoberfläche ein Häutchen von Oxyd oder Schmutz, so ist der erste Funke oft schwach oder er bleibt ganz aus, während man bei Aufhebung des Contacts einen hellen Funken bekommt. Gießt man etwas Wasser auf das Quecksilber, so verliert der Funke bedeutend an Glanz, allein ganz regelmäßig, sowohl bei Vollziehung als bei Aufhebung des Contacts. Macht man die Berührung zwischen blankem Platin, so ist der Funke auch sehr klein, allein gleichmäßig auf beiden Wegen. Indeß ist der wahre elektrische Funke sehr klein, und, wenn man Quecksilberflächen anwendet, wird der größte Theil des Lichts von der Verbrennung dieses Metalls erzeugt. Die mit der Verbrennung des Quecksilbers verknüpften Umstände sind am günstigsten bei Aufhebung des Contacts; denn der Act der Trennung legt blanke Metallflächen bloß, während bei Vollziehung des Contacts oft eine dünne Schicht von Oxyd oder Schmutz dazwischen kommt. Daraus ist die allgemeine Meinung entsprungen, daß der Funke nur bei Aufhebung des Contacts erscheine.
959) In Bezug auf die andere Klasse von Fällen, nämlich die, wo eine chemische Verwandtschaft ausgeübt wird (947), aber keine Fortführung der Kraft in die Ferne stattfindet und kein elektrischer Funke erzeugt wird, ist einleuchtend, daß bei solchen Verbindungen Kräfte der intensivsten Art wirksam, und auf irgend eine Weise in ihrer Wirksamkeit balancirt seyn müssen, da diese Kräfte so unmittelbar und ausschließlich gegen einander gerichtet sind, daß keine Anzeigen von dem mächtigen Elektricitätsstrom, den sie erzeugen können, zum Vorschein kommen, wiewohl derselbe Endzustand der
[40] Dinge erhalten wird, wie wenn ein Strom übergegangen wäre. Es war, ich glaube, Berzelius, welcher zuerst die Wärme- und Lichtentwicklung bei Verbrennungen als Folgen dieser Aeußerungsweise der elektrischen Kräfte der sich verbindenden Theilchen ansah. Allein wir bedürfen einer genaueren und ausgedehnteren Kenntniß von der Natur der Elektricität, und von der Art, wie sie den Atomen der Materie beigesellt ist, ehe wir die Wirkung dieser, die Atome so vereinigende Kraft einsehen, und die Natur des großen Unterschiedes, welchen sie in den beiden so eben unterschiedenen Wirkungsweisen darbietet, begreifen können. Wir können uns Gedanken darüber machen, aber diese sind zur Zeit unter die große Masse zweifelhafter Kenntnisse (876) zu rechnen, welche wir eher zu verringern als zu vermehren suchen müssen; denn die vielen Widersprüche in diesen Kenntnissen selbst zeigen, daß sich nur ein kleiner Theil von ihnen zuletzt als wahr erweisen kann.
960) Von den beiden Wirkungsweisen der chemischen Verwandtschaft ist es wichtig zu bemerken, daß die, welche den elektrischen Strom erzeugt, eben so, bestimmt in ihren Wirkungen ist als die, welche die gewöhnlichen chemischen Verbindungen hervorbringt, so daß wenn man die Erzeugung oder Entwicklung der Elektricität bei Verbindungen oder Zersetzungen untersucht, es nöthig ist, nicht bloß gewisse, von einem Elektricitätsstrom abhängige Effecte zu beachten, sondern auch deren Menge; und wiewohl in einzelnen Fällen von chemischer Action die dabei thätigen Kräfte zum Theil auf die eine, zum Theil auf die andere Weise ausgeübt werden, so sind es doch nur die zur Erzeugung des Stromes wirksamen, welche eine Beziehung zur voltaschen Action haben. So sind, wenn sich Sauerstoff und Wasserstoff zu Wasser verbinden, elektrische Kräfte von der ungeheuersten Größe thätig (861. 873); allein auf welche erdenkliche Weise auch bis jetzt die Flamme, welche sie bei ihrer energischen Verbindung erzeugen, untersucht [41] worden ist, so hat man doch nur höchst geringe Spuren (von jenen Kräften) aufgefunden. Diese (Spuren) können daher nicht als Beweise von der Natur der Wirkung angesehen werden, sondern sind nur zufällig, und in Bezug auf die thätigen Kräfte unvergleichlich klein; sie geben keinen Aufschluß über die Art, wie die Theilchen auf einander wirken, oder wie ihre Kräfte zuletzt angeordnet werden.
961) Daß solche chemische Actionen keinen elektrischen Strom erzeugen, stimmt völlig mit dem, was wir vom voltaschen Apparate wissen, bei welchem es wesentlich ist, daß eins der sich verbindenden Elemente einen Theil von einem elektrolytischen Leiter ausmache oder in directer Beziehung zu ihm stehe (921. 923). Daß solche Fälle keine freie Spannungs-Elektricität erzeugen, und daß sie dagegen, wenn sie in voltasche Actionen verwandelt werden, einen Strom liefern, in welchem die entgegengesetzten Kräfte so gleich sind um einander zu neutralisiren, beweist die Gleichheit der Kräfte in den gegen einander wirkenden Körpertheilchen, und deshalb die Gleichheit von elektrischen Kräften in denjenigen Quantitäten der Substanzen, welche elektro-chemische Aequivalente genannt werden (824). Dieß ist ein fernerer Beweis, daß die elektro-chemische Action (783 etc.) bestimmter Natur ist, und daß die chemische Verwandtschaft und die Elektricität ein und dieselbe Kraft ausmachen (917 etc.).
962) Die directe Beziehung der Wirkungen, welche in der voltasche Säule an dem Orte der experimentellen Zersetzung ausgeübt werden, zu den chemischen Verwandtschaften, die an dem Orte der Erregung thätig sind (891. 917), giebt eine sehr einfache und natürliche Ansicht von der Ursache, weshalb die entwickelten Körper oder Ionen in gewissen Richtungen wandern: denn nur wenn sie in diesen Richtungen wandern, sind ihre Kräfte im Stande, neben den überlegenen Kräften, die an dem Orte, wo die Wirkung des Ganzen bedingt wird, [42] vorwalten, zu bestehen und sie zu compensiren (wenigstens in Richtung). Wenn z. B. in einer voltaschen Kette, deren Thätigkeit durch die Anziehung des Zinks zum Sauerstoff des Wassers bedingt wird, das Zink von rechts nach links wandert, so wird jedes andere in die Kette eingeschlossene Kation, welches ein Theil eines Elektrolyten ist oder in dem Moment einen Theil eines solchen ausmacht, sich auch von der Rechten zur Linken bewegen; und wie der Sauerstoff des Wassers sich, vermöge seiner natürlichen Verwandtschaft zum Zink, von der Linken zur Rechten bewegt, so wird auch jeder andere Körper, der in dieselbe Klasse gehört (d. h. jedes andere Anion) und zur Zeit unter seiner Herrschaft steht, sich von der Linken zur Rechten bewegen.
963) Dieß läßt sich durch Fig. 11 Taf. I erläutern, wo der doppelte Kreis eine geschlossene voltasche Kette vorstellen mag, deren Kräfte bestimmt sind, wenn wir für einen Moment annehmen, das Zink und das Platin seyen Platten von den auf das Wasser , und andere Substanzen einwirkenden Metallen, deren Wirksamkeit jedoch durch Anwendung einer Batterie bei (989) so verstärkt worden, daß sie verschiedene Zersetzungen hervorbringen. Diese Annahme ist erlaubt, weil die Wirkung der Batterie nur in einer Wiederholung dessen besteht, was zwischen und vorgeht, im Fall und wirklich nur ein einfaches Plattenpaar ausmachen. Das Zink und der Sauerstoff suchen sich, vermöge ihrer gegenseitigen Verwandtschaft, mit einander zu verbinden, allein da der Sauerstoff bereits mit dem Wasserstoff verbunden ist, und die ihm einwohnenden chemischen Kräfte zur Zeit neutralisirt sind durch die des Wasserstoffs, so muß dieser Wasserstoff den Sauerstoff verlassen, und in Richtung des Pfeiles vorschreiten; sonst kann das Zink sich nicht in derselben Richtung bewegen, um sich mit dem Sauerstoff zu verbinden, noch kann sich der Sauerstoff in der entgegengesetzten [43] Richtung bewegen, um sich mit dem Zink zu verbinden, da die Relation der ähnlichen Kräfte von und zu den entgegengesetzten Kräften von dieß verhindert. So wie der Wasserstoff vorrückt und bei dem, einen Theil der Kette ausmachenden Platin anlangt, theilt er durch dieses seine elektrischen oder chemischen Kräfte dem nächsten Elektrolyt in der Kette mit, nämlich dem geschmolzenen Chlorblei , dessen Chlor, in Uebereinstimmung mit der Richtung des Sauerstoffs, bei wandern muß, denn es hat die Kräfte zu compensiren, die in seinem Theil der Kette gestört sind durch den überwiegenden Einfluß der durch die Batterie unterstützten Kräfte zwischen dem Sauerstoff und Zink bei , ; und aus einem ähnlichen Grunde muß das Blei in der durch den Pfeil angedeuteten Richtung wandern, damit es zu dem ersten bewegenden Körper seiner eigenen Klasse, nämlich dem Zink in richtige Relation komme. Wenn Kupfer von bis in den Bogen kommt, wirkt es, wie es früher das Platin that, und wenn bei , ein anderer Elektrolyt, z. B. Jodzinn, vorhanden ist, so muß das Jod , als ein Anion, sich übereinstimmend mit dem erregenden Anion, nämlich dem Sauerstoff bewegen, und das Kation Zinn wandert in Uebereinstimmung mit den übrigen Kationen , und , damit längs dem ganzen Bogen die chemischen Kräfte, sowohl ihrer Richtung als ihrer Menge nach, im Gleichgewicht seyen. Sind die Anionen fähig bei ihrer Circulation sich mit den Metallen an den Anoden der respectiven Elektrolyte zu verbinden, wie es beim Platin und beim Kupfer der Fall seyn würde, so werden diese Körper Theile der Elektrolyte, und wandern sogleich unter dem Einfluß des Stroms; allein wegen ihrer Relation zum Zink ist es offenbar unmöglich, daß sie in anderer Richtung wandern können als in der, welche mit dessen Lauf übereinstimmt, und deshalb können sie nicht anders als von der Anode zu der Kathode überzugehen suchen.
[44] 964) Bei einem Kreise, wie der gezeichnete, lassen sich daher alle bekannten Anionen innerhalb, und alle Kationen außerhalb zusammenstellen. Wenn irgend eine Anzahl derselben als Ionen in die Constitution der Elektrolyten eintritt, und sie, Einen Bogen bildend, gleichzeitig Einem gemeinschaftlichen Strom unterworfen sind, so müssen die Anionen, in Uebereinstimmung mit einander, in der einen Richtung, und die Kationen in der entgegengesetzten wandern. Noch mehr! Es müssen aequivalente Mengen dieser Körper in entgegengesetzten Richtungen wandern. Das Vorrücken von jeden 32,5 Theilen Zink muß begleitet seyn von einem Zurückweichen von 8 Theilen Sauerstoff bei , von 36 Theilen Chlor bei , von 126 Theilen Jod bei ; so wie von einem Vorschreiten elektro-chemischer Aequivalente von Wasserstoff, Blei, Kupfer und Zinn, bei , , und .
965) Nimmt man den gegenwärtigen Aufsatz für einen richtigen Ausdruck der Thatsachen, so wird er doch nur eine Bestätigung gewisser allgemeiner Ansichten seyn, welche Humphry Davy in seiner Baker’schen Vorlesung von 1806 ausgesprochen[10], und i. J. 1826 in einer andern Baker’sehen Vorlesung verbessert aufgestellt hat[11]. Sein allgemeiner Satz ist der: Chemische und elektrische Anziehungen werden durch die nämliche Ursache erzeugt, die in dem einen Fall auf Theilchen, in dem andern auf Massen von Substanz einwirkt; und ein und dieselbe Eigenschaft, verschiedentlich abgeändert, ist die Ursache aller Erscheinungen bei den verschiedenen voltaschen Combinationen [12]. Diesen Satz halte ich für wahr; allein indem ich ihn annehme und vertheidige,
[45] muß ich mich gegen die Voraussetzung verwahren, als wollte ich Allem, was damit in jenen beiden Aufsätzen verknüpft ist, beistimmen oder die Experimente, welche daselbst als entscheidende Beweise der Wahrheit des Salzes angeführt werden, gutheißen. Wäre dieß meine Meinung gewesen, würde ich diese Untersuchungen nicht unternommen haben. Vielleicht glauben Einige, ich wäre verpflichtet gewesen, jene Aufsätze durchzugehen, das, was ich anerkenne, von dem, was ich verwerfe, zu unterscheiden, und für beide Fälle gute experimentelle oder philosophische Beweise anzuführen; allein dann wäre ich auch gezwungen gewesen, Alles, was für und wider die Nothwendigkeit des Metallcontacts, für und wider den Ursprung der voltaschen Elektricität bei chemischen Actionen geschrieben worden ist, ebenfalls zu recensiren, und diese Arbeit mochte ich nicht im gegenwärtigen Aufsatz unternehmen[13].
966) Zum Verständniß mancher Umstände bei der voltaschen Action wurde erfordert, wo möglich entscheidend zu bestimmen, ob Elektrolyte der Wirkung eines elektrischen Stroms unterhalb einer gewissen Intensität widerstehen können? – ob die Intensität, bei welcher der Strom zu wirken aufhört, gleich sey für alle Körper? – und ob die so der Elektrolysirung widerstehenden Körper, nachdem sie aufgehört den elektrischen Strom als Elektrolyte zu leiten, denselben nach Art der Metalle leiten oder sich als vollkommene Isolatoren verhalten?
967) Aus den (904. 906) beschriebenen Versuchen ist einleuchtend, daß verschiedene Körper mit sehr verschiedener Leichtigkeit zersetzt werden, und daß sie anscheinend zu ihrer Zersetzung Ströme von verschiedener Intensität erfordern, indem sie einigen widerstehen, andern unterliegen. Allein es war nothwendig, durch sehr sorgfältige und besondere Versuche auszumachen, ob ein Strom wirklich durch einen Elektrolyten gehen könne, ohne ihn zu zersetzen (910).
968) Es wurde die Vorrichtung, Fig. 12 Taf. I, gemacht, bestehend aus zwei Glasgefäßen mit verdünnter Schwefelsäure vom specifischen Gewicht 1,25. Die Platte war amalgamirtes Zink, verbunden durch den Platindraht mit der Platinplatte . Der Platindraht verband die beiden Platinplatten , und der Platindraht saß an der Platinplatte . Auf die Platte war ein [223] mit Jodkalium-Lösung befeuchtetes Papier gelegt. Der Draht war so gebogen, daß man ihn nach Belieben mit seinem Ende auf diesem Papiere ruhen, und dann durch die Jodabscheidung den etwaigen Durchgang eines Stroms angeben, oder, nachdem er in die punktirte Lage gebracht, in directe Verbindung mit der Platinplatte treten, und so die Elektricität ohne bewirkte Zersetzung überleiten lassen konnte. Der Zweck dabei war, durch die Wirkung der Säure auf das amalgamirte Zink im ersten Gefäß einen Strom zu erregen, ihn mittelst der Platin-Elektroden durch die Säure im zweiten Gefäß zu leiten (damit seine etwaige wasserzersetzende Kraft beobachtet werden könnte) und seine Anwesenheit nach Belieben durch die Zersetzung bei zu ermitteln, ohne ihm beständig das Hinderniß entgegenzusetzen, welches entstanden seyn würde, wenn man ihn dort fortwährend eine Zersetzung hätte bewirken lassen. Zu Anfang des Versuchs wurde der Draht auf das Papier gesetzt, wo dann bei eine Zersetzung eintrat; und darauf wurde er auf dem entblößten Theil der Platte stehen gelassen, so daß eine beständige metallische Berührung stattfand.
969) Nach mehren Stunden wurde das Drahtende wieder auf das Probepapier bei gestellt; es trat eine Zersetzung ein, und der Uebergang des Stroms war also vollkommen erwiesen. Nur war der Strom nun, verglichen mit seiner Stärke zu Anfange des Versuchs, sehr schwach, in Folge eines besonderen Zustandes, welchen die Metallflächen im zweiten Gefäße angenommen hatten, und vermöge dessen sie dem Durchgang des Stroms einen Widerstand entgegensetzten (1040). Indeß erwieß sich durch die Zersetzung, daß dieser Zustand der Platten im zweiten Gefäße nicht fähig war, den im ersten Gefäß erregten Strom ganz zu hemmen, und weiter war nichts in der gegenwärtigen Untersuchung zu ermitteln nothwendig.
970) Von Zeit zu Zeit wurde dieser Apparat untersucht; [224] allein zwölf Tage lang, währenddeß das Wasser im zweiten Gefäß beständig seiner Wirkung ausgesetzt gewesen war, fand immer eine Circulation von einem elektrischen Strome statt. Ungeachtet dieser langen Zeit kam nicht die geringste Anzeige von Gasblasen auf einer der Platten in diesem Gefäße zum Vorschein. Hieraus schließe ich, daß wirklich ein Strom übergegangen war, aber einer von geringerem Stärkegrad als der, bei welchem die Bestandtheile des Wassers ohne Hülfe einer secundären Kraft, wie sie aus der Verbindbarkeit derselben mit der Substanz der Elektroden oder mit der umgebenden Flüssigkeit entspringt, sich trennen.
971) Man könnte meinen, Sauerstoff und Wasserstoff wären in so geringen Mengen entwickelt worden, daß sie sich gänzlich in Wasser lösten und endlich an der Oberfläche entwichen oder sich wieder zu Wasser vereinigten. Daß der Wasserstoff so gelöst werden könne, zeigte sich im ersten Gefäß; denn nach mehren Tagen erschienen auf einem Glasstab, der zur Auseinanderhaltung des Zinks und Platins eingesteckt worden war, und auf dem Platin selbst, allmälig kleine Gasblasen, und diese bestanden aus Wasserstoff. Ihre Entstehung war die, daß das Zink, ungeachtet seiner Amalgamation, eine kleine directe Einwirkung von der Säure erlitt, wodurch von seiner Oberfläche beständig ein kleiner Strom von Gasblasen aufstieg; ein kleiner Theil dieses Wasserstoffs löste sich allmälig in verdünnter Säure, und wurde zum Theil an der Oberfläche des Stabes und der Platte in Freiheit gesetzt, gemäß der wohl bekannten Einwirkung solcher starren Körper auf Lösungen von Gasen (623. etc.).
972) Allein wären im zweiten Gefäße die Gase durch Zersetzung des Wassers entwickelt und hätten sie gesucht sich zu lösen, so würde auch mit allem Grund zu erwarten gewesen seyn, daß einige Blasen an den Elektroden zum Vorschein gekommen wären, besonders an der negativen, wenn auch nur wegen deren Wirkung [225] als ein festes Korn auf die vermeintliche Lösung. Allein es erschien selbst nach zwölf Tagen keine Blase.
973) Sobald indeß nur einige Tropfen Salpetersäure in das Gefäß , Fig. 12 Taf. I, geschüttet wurden, waren die Resultate ganz anders. In weniger als fünf Minuten erschienen dann Gasblasen an den Platten und im zweiten Gefäß. Um zu beweisen, daß dieß die Wirkung des elektrischen Stroms sey (dessen Uebergang zugleich aus der Probe bei hervorging), wurde die Verbindung bei unterbrochen, die Platten von Blasen gereinigt und 15 Minuten lang in der Säure des Gefäßes gelassen. Während dieser Zeit erschienen keine Blasen auf ihnen. Allein nach Wiederherstellung der Verbindung bei verstrich nicht eine Minute als schon Gas auf den Platten erschien. Es ist also vollkommen bewiesen, daß der im Gefäß durch verdünnte Schwefelsäure mit Zusatz von etwas Salpetersäure erregte Strom Intensität genug besaß, um die chemische Verwandtschaft zwischen dem Sauerstoff und Wasserstoff des Wassers im Gefäße zu überwinden, während der durch Schwefelsäure allein erregte Strom nicht stark genug dazu war.
974) Als eine starke Lösung von Aetzkali in dem Gefäße zur Erregung des Stromes angewandt wurde, fand sich durch die Zersetzung bei , daß wirklich ein Strom überging. Allein er hatte nicht Stärke genug, um das Wasser im Gefäß zu zersetzen. Denn wiewohl der Apparat 14 Tage stehen blieb, und während der ganzen Zeit Beweise von dem Uebergange des Stromes gab, so erschien doch nicht das mindeste Gas an den Platten , noch sonst eine Anzeige von geschehener Wasserzersetzung.
975) Nun wurde mit einer Lösung von schwefelsaurem Natron experimentirt, um zu ermitteln, ob zu dessen Zersetzung auch eine gewisse elektrolytische Intensität erforderlich sey, wie es so eben für das Wasser festgestellt [226] worden (974). Der Apparat war wie Fig. 13 Taf. I eingerichtet. ist eine Platin- und eine Zinkplatte, beide eingetaucht in eine Kochsalzlösung; und sind Platinplatten, die durch Platindrähte (ausgenommen in dem Galvanometer ) mit und verbunden sind, ist ein platiner Verbindungsdraht, der mit seinen Enden entweder auf die Platten und oder auf die darauf liegenden, mit Lösungen getränkten Papiere gesetzt wird, so daß man den Strom entweder ohne Zersetzung oder mit einer oder zwei Zersetzungen, wie es das Bedürfniß erforderte, übergehen lassen konnte. Um mit den Anoden und Kathoden an den Zersetzungsstellen wechseln zu können, wurde dem Apparat zuweilen die Einrichtung Fig. 14 gegeben. Hier wurde nur eine Platinplatte angewandt, und beide Papierstücke, auf denen die Zersetzung vorgenommen werden sollte, wurden auf dieselbe gelegt; die Drähte von und standen entweder auf diesen Papierstücken, oder auf der Platte , je nachdem der Strom mit oder ohne Zersetzung der Lösungen erforderlich war.
976) Als an eine Zersetzungsstelle eine Lösung von Jodkalium und an die andere eine von schwefelsaurem Natron gebracht wurde, so daß der elektrische Strom zugleich durch beide Lösungen gehen mußte, wurde die Jodidlösung langsam zersetzt, unter Abscheidung von Jod an der Anode, und von Alkali an der Kathode; allein die Lösung von schwefelsaurem Natron gab keine Anzeigen von Zersetzung, schied weder Alkali noch Säure aus. Als die Drähte so gestellt wurden, daß die Jodidlösung allein der Wirkung des Stromes ausgesetzt war (900), wurde sie rasch und mächtig zersetzt; allein als ich den Drähten eine solche Stellung gab, daß bloß das Glaubersalz unter der Wirkung war, widerstand es auch jetzt der Zersetzung. Endlich wurde der Apparat so eingerichtet, zwölf Stunden lang unter einer Glasglocke stehen gelassen, während welcher ganzen Zeit der Strom [227] fortwährend durch die Glaubersalzlösung ging, die nur in zwei Lagen Lackmus- und Kurkumä-Fließpapier enthalten war. Nach Verlauf dieser Zeit ergab sich aus der Zersetzung der an der zweiten Zersetzungsstelle befindlichen Jodidlösung, daß der Strom noch überging und zwölf Stunden lang übergegangen war, doch hatte sich keine Spur von Säure oder Alkali aus dem schwefelsauren Natron abgeschieden.
977) Aus diesen Versuchen kann, glaube ich, geschlossen werden, daß eine Lösung von schwefelsaurem Natron einen Elektricitätsstrom zu leiten vermag, welcher unfähig ist dieß Salz zu zersetzen; daß dieß Salz im Zustande der Lösung, wie das Wasser, eine gewisse elektrolytische Intensität zu seiner Zersetzung erfordert, und zwar eine weit höhere, als das Jodkalium in einem ähnlichen Zustand von Lösung.
978) Ich experimentirte nun mit Körpern, die durch Schmelzung zersetzbar gemacht werden, und zwar zuerst mit Chlorblei. Der Strom wurde durch Schwefelsäure, ohne Salpetersäure, zwischen einer Zink- und einer Platinplatte erregt (Fig. 15), und dann successiv geleitet durch etwas Chlorblei, geschmolzen auf Glas bei , durch ein mit Jodkaliumlösung befeuchtetes Papier bei , und durch ein Galvanometer bei . Der Draht war von Platin. Bei dieser Vorrichtung zeigten die Zersetzung bei , und die Ablenkung bei , daß ein Strom überging, allein bei kam keine Zersetzung zum Vorschein, selbst nicht als bei eine metallische Communication hergestellt ward. Der Versuch wurde mit gleichem Erfolge mehrmals wiederholt, und ich schließe daraus, daß in diesem Fall der Strom nicht intensiv genug war, um das Chlorblei zu zersetzen, und ferner, daß das geschmolzene Chlorblei, wie das Wasser (974) einen elektrischen Strom zu leiten vermag, der nicht so intensiv ist als zu seiner Zersetzung erfordert wird.
979) Nun wurde Chlorsilber statt des Chlorbleis [228] bei , Fig. 15, angebracht. Jetzt zeigte sich eine sehr rasche Zersetzung der Jodkalium-Lösung bei , und, als daselbst eine metallische Communication hergestellt wurde, eine sehr beträchtliche Ablenkung der Galvanometernadel bei . Es schien auch Platin an der Anode des geschmolzenen Chlorsilbers bei gelöst zu werden, und alle Anzeigen einer daselbst eingetretenen Zersetzung waren sichtbar.
980) Ein fernerer Beweis von der Zersetzung wurde auf folgende Weise erhalten. Ich brachte die Platindrähte in dem geschmolzenen Chlorid bei sehr nahe an einander, und ließ sie so, während bei eine metallische Communication hergestellt war. Die Ablenkung des Galvanometers zeigte den Uebergang eines Stromes an, eines zwar schwachen, aber constanten. Nach einer oder zwei Minuten wurde die Nadel indeß plötzlich sehr heftig ergriffen, und sie zeigte einen eben so starken Strom an, wie wenn bei Metallcontact stattgefunden hätte. Und wirklich war dieß auch der Fall, denn das durch den Strom reducirte Silber war in langen zarten Nadeln krystallisirt, die zuletzt die metallische Communication herstellten; und so wie sie einen kräftigeren Strom durchließen als das geschmolzene Chlorid, so bewiesen sie zugleich, daß das Chlorid eine elektrochemische Zersetzung erlitten hatte. Hieraus erhellt, daß der Strom, welcher durch verdünnte Schwefelsäure zwischen Zink und Platin erregt wird, eine größere Intensität besitzt als zur Elektrolysirung von geschmolzenem Chlorsilber, wenn es sich zwischen Platin-Elektroden befindet, erfordert wird, obgleich er nicht intensiv genug ist, um unter denselben Umständen Chlorblei zu zersetzen.
981) Ein Tropfen Wasser, statt der geschmolzenen Chloride bei angebracht, zeigte, wie in dem früheren Fall (970), daß es einen zu seiner Zersetzung unzulänglichen Strom leiten könne, denn zugleich trat nach einiger Zeit bei eine Zersetzung der Jodidlösung [229] ein. Allein seine Leitungsfähigkeit war viel geringer als die des geschmolzenen Chlorbleis (978).
982) Geschmolzener Salpeter leitete etwas besser. Ich vermochte nicht mit Gewißheit zu entscheiden, ob er elektrolysirt wurde; allein ich vermuthe nicht, denn am Platin an der Kathode fand keine Entfärbung statt. Wäre Schwefel-Salpetersäure in dem Erregungsgefäße angewandt worden, würden Salpeter und Chlorblei eine Zersetzung erlitten haben, wie das Wasser.
983) Diese Beispiele von Leitung ohne Zersetzung und die Nothwendigkeit einer gewissen elektrolytischen Intensität zur Trennung der Ionen verschiedener Elektrolyte stehen im unmittelbaren Zusammenhange mit den Versuchen und Resultaten, die im §. 10 der vierten Reihe dieser Untersuchungen (418. 423. 444. 449)[14] gegeben worden sind. Allein es ist in Bezug sowohl auf den ersten Ursprung des elektrischen Stroms, als auf die Weise, in welcher dieser durch die Dazwischenkunft größerer oder kleiner Strecken schlechter, entweder zersetzbarer oder nicht zersetzbarer Leiter geschwächt wird, eine genauere Kenntniß der Natur der Intensität erforderlich, ehe jener Zusammenhang im Einzelnen und vollständig verstanden werden kann.
984) Beim Wasser scheinen die bis jetzt von mir angestellten Versuche zu zeigen, daß wenn der elektrische Strom auf eine geringere als die zur Zersetzung desselben erforderliche Intensität geschwächt worden ist, der Grad der Leitung derselbe bleibt, es mag Schwefelsäure oder irgend einer der vielen Körper, welche seine Ueberführungskraft als Elektrolyt abändern, zugegen seyn oder nicht; oder mit anderen Worten, daß die für das Wasser erforderliche elektrolytische Intensität gleich ist, das Wasser mag rein oder durch Zusatz einer jener Substanzen leitender gemacht worden seyn; und daß das Wasser, es mag rein oder gesäuert seyn, für Ströme von geringerer [230] Intensität als die eben genannte ein gleiches Leitungsvermögen besitzt. Ein Apparat wie Fig. 12 wurde zusammengestellt, mit Schwefelsäure im Gefäße und reinem destillirten Wasser im Gefäß . Aus der Zersetzung bei schien es, wie wenn das Wasser für einen Strom von so geringer Intensität, daß er keine Zersetzung bewirkt, ein besserer Leiter sey als verdünnte Schwefelsäure. Ich bin jedoch geneigt, diese scheinbar bessere Leitung des Wassers von Veränderungen in jenem eigenthümlichen weiterhin (1040) beschriebenen Zustand der Platin-Elektrode herzuleiten, welchen diese, so weit ich sehe, in verdünnter Schwefelsäure in höherem Grade annehmen als in reinem Wasser. Das den Säuren, Alkalien, Salzen und anderen gelösten Körpern eigenthümliche Vermögen, die Leitungsfähigkeit zu erhöhen, scheint nur in den Fällen, wo der dem Strom unterworfene Elektrolyt eine Zersetzung erleidet, Stand zu halten, und dagegen allen Einfluß zu verlieren, wenn der durchgelassene Strom zu schwach ist, um eine chemische Veränderung zu bewirken. Wahrscheinlich besitzt ein Elektrolyt im starren Zustande (419) ein gleiches Leitungsvermögen wie im flüssigen Zustande für Ströme von geringerer als der erforderlichen elektrolytischen Intensität.
985) Elektricitätsströme, hervorgebracht durch weniger als acht bis zehn Plattenpaaren (series of voltaic elements), lassen sich auf die Intensität, bei welcher sie vom Wasser ohne Zersetzung geleitet worden, dadurch zurückführen, daß man sie durch drei oder vier Gefäße leitet, worin Wasser zwischen Platinflächen enthalten ist. Die Principien der Schwächung (principles of interference), auf denen diese Wirkungen beruhen, werden weiterhin beschrieben werden (1009. 1018); allein das Verfahren kann nützlich seyn, um Ströme von Normalstärke zu erhalten, und ist wahrscheinlich auf Batterien von jeglicher Zahl von Plattenpaaren anwendbar.
[231] 986) Da wir aller Wahrscheinlichkeit nach in Zukunft finden werden, daß alle Elektrolyte einen elektrischen Strom von gewisser Intensität zu ihrer Zersetzung erfordern, sie aber in dem dazu erforderlichen Grad von Intensität verschieden sind, so wird es wünschenswerth, sie nach dem Grade ihrer elektrolytischen Intensitäten in einer Tafel zusammenzustellen. Ehe aber eine solche Tafel construirt werden kann, müssen Untersuchungen über diesen Punkt jedoch sehr weit ausgedehnt werden; und darin eine größere Zahl von Körpern eingeschlossen werden als bisher erwähnt wurde. Bei solchen Versuchen wird es besonders nützlich seyn, die Natur der angewandten Elektrode zu beschreiben, oder wo möglich solche auszuwählen, welche, wie Platin und Graphit, in gewissen Fällen, nicht fähig sind, die Trennung der abzuscheidenden Ionen zu unterstützen (913).
987) Von den beiden Arten, auf welche Körper die elektrischen Kräfte zu leiten vermögen, nämlich der, welche die Metalle so charakteristisch zeigen, und der, welche mit einer Zersetzung begleitet ist, scheint die erste allen Körpern gemein zu seyn, wiewohl in einem fast unendlichen Grad von Verschiedenheit; die zweite aber ist bis jetzt bloß bei den Elektrolyten angetroffen. Es ist jedoch möglich, daß man sie künftig auch bei den Metallen auffinden werde; denn deren Fähigkeit, ohne Zersetzung zu leiten, kann vielleicht mit Recht davon abgeleitet werden, daß sie zu ihrer Zersetzung eine sehr hohe elektrolytische Intensität erfordern.
987½) Der Satz, daß eine gewisse elektrolytische Intensität nothwendig erforderlich ist, wenn eine Zersetzung eintreten soll, ist von großer Wichtigkeit bei allen Betrachtungen über die wahrscheinlichen Wirkungen schwacher Ströme, wie sie z. B. durch natürliche Thermo-Elektricität oder natürliche voltasche Ketten hervorgerufen werden. Denn um eine Zersetzung oder Verbindung zu bewirken, muß der Strom nicht bloß da [232] seyn, sondern auch eine gewisse Intensität haben, ehe er die ruhenden, ihm sich widersetzenden Verwandtschaften überwältigen kann, sonst wird er geleitet werden und keine permanenten Effecte bewirken. Andererseits sind nun auch die Grundsätze einleuchtend, nach denen man eine entgegenwirkende Action durch die Juxtaposition solcher Körper, die nicht genug Affinität haben, um direct auf einander einzuwirken (913), wird so schwächen können, daß ein sehr schwacher Strom im Stande ist, chemische Veränderungen herbeizuführen.
988) Indem ich diesen Abschnitt über die zur Elektrolysirung nothwendige Intensität beende, kann ich nicht umhin über die Intensität überhaupt den folgenden merkwürdigen Schluß auszusprechen. Es scheint, daß ein voltascher Strom von einer gewissen Intensität, die von der Stärke der ihn hervorrufenden chemischen Verwandtschaften abhängt (916), einen gegebenen Elektrolyten ohne Beziehung auf die Menge der durchgegangenen Elektricität zersetzen kann, indem die Intensität allein entscheidet, ob der Elektrolyt zersetzt werde oder nicht. Wenn sich dieser Schluß bestätigt, werden wir die Umstände so einrichten können, daß dieselbe Menge von Elektricität übergeht in derselben Zeit durch dieselbe Oberfläche in denselben Körper, in demselben Zustand, und daß sie dabei doch an Intensität verschieden ist, und demgemäß in dem einen Fall zersetzt, in dem andern nicht. Denn nimmt man eine Elektricitätsquelle von einer zum Zersetzen unzureichenden Intensität, und ermittelt die in einer gegebenen Zeit übergegangene Elektricitätsmenge, so ist es leicht eine andere Quelle von zureichender Intensität zu nehmen, und durch Dazwischensetzung schlechter Leiter die Menge der Elektricität auf dasselbe Verhältniß wie im ersten Strom zurückzuführen, und dann werden alle Bedingungen zur Hervorbringung der beschriebenen Resultate erfüllt seyn.
989) Geht man von der Betrachtung einfacher Ketten (875 ff.) zu deren Vereinigung zu einer voltaschen Batterie über, so ist einleuchtend, daß wenn die Sachen so geordnet worden, daß zwei Gruppen von Verwandtschaften, statt gegen einander, wie in Fig. 1 und 4 (880. 891), mit einander wirken müssen, sie dann statt einander zu stören, vielmehr einander unterstützen werden. Dieß ist der einfache Fall bei zwei Plattenpaaren, die zur Bildung Einer Kette angeordnet sind. Bei solchen Anordnungen wird die Thätigkeit des Ganzen bekanntlich erhöht, und wenn man zehn oder hundert oder eine noch größere Anzahl solcher Alternationen zweckmäßig zusammenstellt, wird die Kraft des Ganzen verhältnißmäßig erhöht, und wir erhalten so jenes vortreffliche Instrument zu physikalischen Untersuchungen, die voltasche Batterie.
990) Aus den bereits aufgestellten Grundsätzen von der festen Wirkung ist aber klar, daß die Quantität der Elektricität in dem Strom nicht erhöht werden kann mit Vergrößerung der Quantität des Metalls, welches an jeder neuen Stelle der chemischen Action oxydirt und gelöst wird. Eine einfache Zink-Platin-Kette versetzt, mittelst der Oxydation von 32,5 Gran Zink (868), eben so viel Elektricität in den Zustand eines Stroms, als eine tausend Mal größere Menge, oder nahe fünf Pfund desselben Metalls, durch seine Oxydation in einer regulären Batterie von tausend Plattenpaaren liefern würde. Denn es ist einleuchtend, daß die Elektricität, die in der ersten Zelle vom Zink durch die Säure zum Platin geht, und die von der Zersetzung einer festen Menge Wasser in dieser Zelle begleitet oder gar erzeugt wird, in der zweiten Zelle nicht vom Zink durch die Säure zum Platin gehen kann, ohne nicht dort dieselbe Menge Wasser zu zersetzen und dieselbe Menge Zink zu oxydiren (924. [234] 949). Dasselbe geschieht in allen übrigen Zellen; in jeder muß das elektro-chemische Aequivalent Wasser zersetzt werden, ehe der Strom durch dieselbe gehen kann. Denn die Menge der durchgegangenen Elektricität und die Menge des zersetzten Elektrolyten müssen aequivalent zu einander seyn. Die Wirkung einer jeden Zelle geht also nicht dahin, die in irgend einer Zelle in Bewegung gesetzte Quantität (Elektricität) zu vergrößern, sondern diejenige Quantität (Elektricität) forttreiben zu helfen, deren Uebergang mit der Oxydation des Zinks in dieser Zelle vereinbar ist, und in dieser Weise erhöht sie jene eigenthümliche Eigenschaft des Stroms, welche wir mit dem Namen Intensität bezeichnen, ohne die Quantität zu vermehren, welche der in jeder einzelnen Zelle der ganzen Reihe oxydirten Menge Zinks entspricht.
991) Um dieß zu beweisen stellte ich zehn Plattenpaare von Platin und amalgamirtem Zink mit verdünnter Schwefelsäure zu einer Batterie zusammen. Als ich diese Batterie schloß, wirkten alle Platten, und an den Platinflächen entwickelte sich Gas. Dieß wurde gesammelt, und es fand sich, daß die Menge desselben in allen Zellen gleich war; und eben so stand die Menge des an jeder Platinplatte entwickelten Wasserstoffs in demselben Verhältniß zur Menge des an jeder Zinkplatte gebildeten Oxyds, wie es früher bei dem Versuche mit der einfachen Kette der Fall war (864 etc.). Es war also gewiß, daß gerade so viel, und nicht mehr, Elektricität durch die Reihe von zehn Plattenpaaren durchgegangen war, als durch ein einziges Paar gegangen oder in Bewegung gesetzt seyn würde, ungeachtet im ersten Fall eine zehn Mal größere Menge Zink verbraucht wurde.
992) Diese Wahrheit ist auch schon längst auf einem anderen Wege bewiesen, nämlich durch die Einwirkung des entwickelten Stroms auf eine Magnetnadel. Die ablenkende Kraft eines einzigen Plattenpaares ist nämlich gleich der ablenkenden Kraft der ganzen Batterie, wenn [235] nur die angewandten Drähte dick genug sind, um den Strom eines einzigen Plattenpaars ungehindert zu leiten; allein die Ursache dieser Gleichheit konnte nicht verstanden werden, so lange die feste Wirkung und Entwicklung der Elektricität (783. 869) unbekannt war.
993) Daß die Zersetzungskraft einer Batterie die eines einzigen Plattenpaars übertrifft, ist auf zweifache Weise einleuchtend. Elektrolyte, welche durch eine so starke Verwandtschaft zusammengehalten werden, daß sie dem einfachen Plattenpaar widerstehen, geben ihre Elemente unter dem von vielen Plattenpaaren erregten Strome aus; und ein Körper, welcher durch die Wirkung eines oder einiger wenigen Plattenpaaren zersetzt wird, zerfällt desto leichter in seine Ionen als auf ihn die von einer größeren Zahl von Plattenpaaren erregten Elektricität einwirkt.
994) Beide Wirkungen sind, glaube ich, leicht verständlich. Was auch die Intensität seyn mag (und sie muß natürlicherweise von der Natur der Elektricität abhängen, davon, ob diese aus einer oder mehren Flüssigkeiten bestehe, aus Vibrationen eines Aethers oder irgend einer anderen Art oder einem Zustand von Materie), so ist doch nicht schwierig einzusehen, daß der Grad von Intensität, mit welchem ein Elektricitätsstrom von dem ersten voltaschen Element entwickelt wird, eine Verstärkung erfährt, wenn dieser Strom der Wirkung eines zweiten voltaschen Elements ausgesetzt wird; und da die Zersetzungen bloß widerstrebende Wirkungen sind, aber genau von gleicher Art wie die, welche den Strom erzeugen (917), so scheint es eine natürliche Folgerung, daß die Verwandtschaft, welche der Kraft einer einzelnen Zersetzungswirkung widerstehen kann, unfähig sey den Kräften so vieler Zersetzungswirkungen, wie in der voltaschen Säule gemeinschaftlich thätig sind, Widerstand zu leisten.
995) Daß ein Körper, welcher einem Strom von [236] schwacher Intensität unterliegt, noch leichter einem von größerer Stärke weicht, und dennoch dabei keinen Widerspruch mit dem Gesetz von der festen elektronischen Action darbietet, ist vollkommen erklärlich. Alle Thatsachen, und auch die Theorie, welche ich aufzustellen wagte, zeigen, daß der Act der Zersetzung dem Uebergang des elektrischen Stroms eine gewisse Kraft entgegensetzt; und daß dieser Widerstand mehr oder weniger leicht überwunden wird, in dem Maaße als der zersetzende Strom eine größere oder geringere Kraft besitzt, stimmt mit allen unseren Kenntnissen von dem elektrischen Wesen vollkommen überein.
996) Schon früher (947) habe ich bei der chemischen Einwirkung zwischen Zink und verdünnter Schwefelsäure zwei Theile unterschieden; den, welcher geradezu auf das Zink einwirkt und auf einmal Wasserstoff an dessen Oberfläche entwickelt, und den, welcher, indem er quer durch den vorhandenen Elektrolyten (in diesem Fall: Wasser) eine Anordnung der chemischen Kräfte bewirkt, Sauerstoff aus demselben aufzunehmen sucht, es aber nicht vermag, sobald nicht der darauf folgende elektrische Strom einen freien Durchgang haben, und der Wasserstoff anderswo als am Zink ausgeschieden werden kann. Der elektrische Strom hängt gänzlich von diesem zweiten Theile ab. Allein, wenn der Strom durch Begünstigung der elektrolytischen Action übergehen kann, strebt er, den ersten Theil zu verringern und den letzteren zu vergrößern.
997) Es ist also klar, daß wenn gewöhnliches Zink in einer voltaschen Kette angewandt wird, ein ungeheuerer Verlust an der Kraft stattfindet, welche in die Gestalt eines elektrischen Stroms versetzt werden soll; eine Folgerung, die sehr einleuchten muß, wenn man bedenkt, daß viertehalb Unzen Zink, gehörig oxydirt, Elektricität genug in Umlauf setzen, um fast eine Unze Wasser zu zerlegen und 2400 Kubikzoll Wasserstoffgas zu entwickeln. [237] Dieser Kraftverlust findet nicht nur statt während der Zeit, daß die Elektroden der Batterie in Gemeinschaft stehen, wo er alsdann proportional ist der Wasserstoffmenge, die an der Oberfläche einer der Zinkplatten entwickelt wird, sondern er umschließt auch die gesammte chemische Action, welche stattfindet, wenn die Enden der Säule noch nicht mit einander verbunden sind.
998) Dieser Verlust ist weit größer beim gewöhnlichen Zink als bei reinem, wie Hr. De la Rive gezeigt hat[15]. Die Ursache hievon ist, daß wenn verdünnte Schwefelsäure auf gewöhnliches Zink einwirkt, Theilchen von dem etwa darin vorhandenen Kupfer, Blei, Kadmium und anderen Metallen an seiner Oberfläche enlblößt werden, und daß diese, da sie mit dem Zink in Berührung stehen, kleine sehr wirksame voltasche Ketten bilden, welche eine große Zerstörung des Zinks veranlassen, so wie eine große Entwicklung von Wasserstoff, scheinbar auf der Oberfläche des Zinks, in Wirklichkeit aber auf der Oberfläche dieser beigemengten Metalle. In demselben Verhältniß, da diese zur Entladung der Elektricität oder zur Rückführung derselben zu dem Zink dienen, verringern sie deren Vermögen zur Erzeugung eines Stroms, welcher eine größere Strecke durch die Säure gehen, und nur durch die Kupfer- oder Platinplatte, welche mit dem Zink zur Bildung einer voltaschen Kette verbunden ist, entladen werden soll.
999) Alle diese Uebelstände werden vermieden durch Anwendung eines Zinkamalgams in der von Hrn. Kemp empfohlenen Weise[16] oder durch Anwendung der amalgamirten Platten des Hrn. Sturgeon (863), welcher über die Anwendung derselben zu galvanischen Batterien sagt: Wo es nicht auf die Zerbrechlichkeit und andere mit der Einverleibung des Quecksilbers zum Zink verknüpften [238] Umstände ankommt, würde die Amalgamation der Zinkflächen bei galvanischen Batterien eine wichtige Verbesserung seyn; denn das Metall hält weit länger vor und bleibt eine bedeutende Zeit, selbst mehre Stunden lang glänzend; wesentlich Umstände bei der Anwendung dieses Apparats[17].
1000) Zink, auch unreines, so zubereitet, zersetzt das Wasser der verdünnten Säure nicht merklich, sondern hat eine solche Verwandtschaft zum Sauerstoff, daß in dem Moment, wo es ein Metall, wie Kupfer oder Platin, das wenig oder keine Verwandtschaft hat, in der Säure berührt, einen kräftigen und ergiebigen elektrischen Strom erregt. Wahrscheinlich wirkt das Quecksilber dadurch, daß es vermöge seiner Flüssigkeit die Oberfläche in einen gleichmäßigeren Zustand versetzt, und zwischen einem Ort und dem andern diejenigen kleinen Verschiedenheiten aufhebt, welche zur Bildung der (998) erwähnten kleinen Ketten nöthig sind. Wenn anfänglich in dem Verhältniß von Zink und Quecksilber eine Stelle der Oberfläche verschieden ist von einer andern, so wird die Stelle, wo sich weniger Quecksilber befindet, zuerst angegriffen, und, in Folge der Auflösung von Zink, bald in gleichen Zustand mit der andern versetzt, so daß die ganze Platte auf der Oberfläche gleichförmig wird. Ein Theil derselben kann also nicht als Entlader für einen anderen wirken; und folglich ist die gesammte chemische Kraft auf das Wasser an seiner Oberfläche in demjenigen gleichmäßigen Zustand (949), welcher, wiewohl er einen elektrischen Strom durch die Flüssigkeit zu einer andern, als Entlader (950) dienenden Metallplatte zu erregen trachtet, doch keine Unregelmäßigkeit darbietet, [239] durch die ein Theil mit geringeren Verwandtschaften für den Sauerstoff als Entlader für einen andern wirken könnte. Zwei vortreffliche und wichtige Folgen ergeben sich aus diesem Zustand des Metalls. Die erste ist, daß für die Oxydation einer gewissen Menge Zink das volle Aequivalent von Elektricität erhalten wird, und die zweite: daß eine Batterie, erbaut mit so zubereitetem Zink und geladen mit verdünnter Schwefelsäure, nur so lange thätig ist als die Elektroden in Verbindung stehen, und sogleich zu wirken aufhören, so wie man diese Verbindung unterbricht.
1001) Ich hatte eine kleine Batterie von zehn Plattenpaaren solchergestalt aufgebaut, und bin überzeugt, daß dergleichen Vorrichtungen sehr wichtig seyn werden, besonders für die Entwicklung und Erläuterung der physikalischen Grundsätze dieses Instruments. Als Metalle wandte ich Platin und amalgamirtes Zink an, verbunden mit einander durch angelöthete Platindrähte; der ganze Apparat hatte die Form eines Becher-Apparats (Couronne des Tasses). Die Flüssigkeit war verdünnte Schwefelsäure von dem specifischen Gewicht 1,25. Es fand keine Wirkung auf die Metalle statt, ehe nicht die Elektroden in Gemeinschaft gesetzt waren, und dann war die Wirkung auf das Zink nur proportional der Zersetzung in der Experimentir-Zelle; denn wenn der Strom hier verzögert wurde, wurde er es auch in der Batterie, und es fand keine Vergeudung der Kräfte des Metalles statt.
1002) In Folge dieser Umstände blieb die Säure in den Zellen weit länger wirksam als gewöhnlich. In der That ward sie mit der Zeit nicht merklich schwächer; denn so lange das ihrer Einwirkung ausgesetzte Metall in dem gehörigen Zustand verblieb, behielt auch die Säure fast ihre anfängliche Stärke. Daraus entsprang dann eine Beständigkeit in der Wirkung, welche die mit gewöhnlichem Zink zu erlangende weit übertraf.
[240] 1003) Eine andere vortreffliche Folge ist, daß die Batterie während der Ruhezeit zwischen zwei Versuchen ihren anfänglichen, sehr wirksamen Zustand wieder erlangt. Ein in verdünnte Schwefelsäure eingetauchtes Plattenpaar von Platin und amalgamirtem Zink giebt bei der ersten Schließung einen sehr mächtigen Strom, der aber sogleich sehr viel an Kraft verliert, und zuweilen bis auf ein Achtel oder Zehntel seiner anfänglichen Stärke herabsinkt (1036). Dieß rührt daher, daß die mit Zink in Berührung stehende Säure durch das gebildete Zink neutralisirt, und so eine fortgesetzte schnelle Oxydation des Metalls gehindert wird. Bei gewöhnlichem Zink mischt die Gasentwicklung an dessen Oberfläche alle Flüssigkeit durch einander, und bringt so frische Säure an das Metall, wodurch dann das daselbst gebildete Oxyd entfernt wird. Bei der Batterie von amalgamirtem Zink verbreitet sich, nach jeder Aufhebung des Stroms, die Salzlösung dicht am Zink allmälig in die übrige; und bei Erneuerung des Contacts der Elektroden befinden sich die Zinkplatten unter den günstigsten Umständen zur Erzeugung eines schnellen und mächtigen Stroms.
1004) Auf den ersten Blick könnte man sich einbilden, das amalgamirte Zink wirke wegen des auf seiner Oberfläche befindlichen Quecksilbers weit schwächer als gewöhnliches Zink. Dieß ist aber nicht der Fall. Als der elektrische Strom einer einfachen Kette von Platin und amalgamirtem Zink dem Strom einer andern von Platin und nicht amalgamirtem Zink entgegengestellt ward, war der erstere sehr stark, wiewohl sich an dem amalgamirten kein Gas entwickelte, an dem unamalgamirten aber viel. Wenn ferner, wie Davy gezeigt hat[18], amalgamirtes Zink mit nicht amalgamirtem in Berührung gesetzt, und mit diesem in verdünnte Schwefelsäure oder eine andere erregende Flüssigkeit eingetaucht wird, ist das erstere positiv gegen [241] das letztere, d. h. der Strom geht von dem amalgamirten Zink durch die Flüssigkeit zu dem nicht amalgamirten. Er erklärt dieß, indem er annimmt, »der elektrische Charakter eines Metalles hänge nicht ab von einer inwohnenden und specifischen Eigenschaft, sondern von seinem besonderen Zustande, von jener Form der Aggregation, welche dasselbe zur chemischen Veränderung geschickt mache.«
1005) Die Vorzüglichkeit des amalgamirten Zinks hängt indeß nicht von einer solchen Ursache ab, sondern ist eine sehr einfache Folge des Zustande der mit demselben in Berührung stehenden Flüssigkeit; denn da das unamalgamirte Zink direct und für sich auf die Flüssigkeit wirkt, das amalgamirte aber nicht, neutralisirt das erste (durch das aus ihm gebildete Oxyd) die Säure an seiner Oberfläche, so daß der Proceß der Oxydation verzögert wird, während an der Oberfläche des amalgamirten Zinks das gebildete Oxyd augenblicklich durch vorhandene freie Säure entfernt wird, und die blanke Metallfläche immer bereit steht, mit voller Kraft auf das Wasser zu wirken. Hieraus dann seine größere Wirksamkeit (1037).
1006) Der Gang zur Vervollkommnung der voltaschen Batterie und ihrer Anwendung wird gegenwärtig offenbar ein umgekehrter seyn wie vor wenigen Jahren; denn statt die Anzahl der Platten, die Stärke der Säure und den ganzen Umfang des Instruments zu vermehren, wird man dasselbe mehr auf seinen anfänglichen Zustand von Einfachheit zurückzubringen haben, jedoch mit einer richtigeren Kenntniß und Anwendung der Principien, welche dessen Kraft und Wirksamkeit bedingen. Mit zehn Plattenpaaren können jetzt Zersetzungen bewirkt werden (417), die sonst 500 und 1000 Plattenpaare erforderten. Die Möglichkeit, geschmolzene Chloride, Jodide und andere Verbindungen nach dem zuvor (380 etc.) aufgestellten Gesetz zu zerlegen, und die Gelegenheit, mit Apparaten [242] wie die beschriebenen (769. 814 etc.), gewisse Producte ohne Verlust zu sammeln, macht es wahrscheinlich, daß die voltasche Säule ein nützliches und selbst ökonomisch technisches Instrument werde. Denn die Theorie läßt offenbar schließen, daß man ein Aequivalent einer seltenen Substanz auf Kosten von drei oder vier Aequivalenten einer sehr gemeinen Substanz, z. B. Zink, werde erhalten können, und die Praxis scheint diese Erwartung zu rechtfertigen. Unter diesem Gesichtspunkt halte ich es für sehr wahrscheinlich, daß Platten von Platin oder Silber statt Platten von Kupfer mit Vortheil angewandt, und selbst die mit der Auflösung des Kupfers und seiner Fällung auf das Zink (wodurch die elektromotorische Kraft des Zinks so sehr geschwächt wird) verknüpften Uebelstände vermieden werden können (1047).
1007) Den an der Zersetzungsstelle eintretenden Widerstand gegen die wirkende Kraft an dem Erregungsort habe ich bereits durch die möglichst einfache Form des Experiments erläutert (891. 910). Jetzt beabsichtige ich, die Effecte dieses Widerstands allgemeiner zu untersuchen, jedoch mehr in practischer Beziehung zu den Wirkungen und Erscheinungen der voltaschen Batterie, als in der Absicht jetzt eine strenge und physikalische Darstellung ihrer Natur zu liefern. Die allgemeine und hauptsächliche Ursache dieser Erscheinungen ist der Widerstand gegen die chemischen Zersetzungen; allein außerdem wirken viele andere Umstände mit ein (1034. 1040 etc.), von denen jeder genau muß untersucht worden seyn, ehe eine richtige Erklärung gegeben werden kann.
1008) Da es zweckmäßig seyn wird, die Experimente in einer andern Form zu beschreiben als in welcher [243] sie angestellt wurden, so will ich beide Formen erst erläutern. Platten von Platin, Kupfer, Zink und anderen Metallen, drei Viertelzoll breit und drei Zoll lang, wurden durch angelöthete Platindrähte paarweise mit einander verbunden (Fig. 16 Taf. I), die Platten eines Paars waren gleich oder verschieden, wie es erfordert wurde. Die Platten wurden in Gläser (Fig. 17) gestellt, so daß sie einen voltaschen Tassenkranz bildeten. Einfache Platten wurden angewandt, um die Reihe zu schließen und mit einem Galvanometer oder einem Zersetzungsapparat oder mit beiden zu verbinden. Wenn man nun Fig. 18 mit Fig. 19 vergleicht, kann die letztere als die einfachste Form von der ersteren angesehen werden, denn die Gefäße I, II, III der ersteren sind durch die Zellen I, II, III der letzteren vorgestellt, und die Metallplatten und in der ersteren durch ähnliche Platten und in der letzteren. Der einzige Unterschied zwischen dem Apparat Fig. 18 und dem Trog Fig. 19 besteht darin, daß im ersteren die Berührungsfläche zwischen Metall und Säure doppelt so groß ist wie im letzteren.
1009) Wenn die äußeren Platten der Vorrichtung Fig. 18 durch das Galvanometer metallisch mit einander verbunden sind, besteht das Ganze aus einer Batterie von zwei Paaren Zink-Platin-Platten, die einen Strom vorwärts treiben, welcher aber Wasser ohne Hülfe einer directen chemischen Verwandtschaft zersetzen muß, ehe er durch die Zelle III dringen und folglich auch ehe er circuliren kann. Diese Wasserzersetzung, welche sich dem Uebergang des Stroms widersetzt, kann nach Gefallen als stattfindend an den Oberflächen der beiden die Elektroden in der Zelle III bildenden Platinplatten oder an den beiden Oberflächen der die Zellen II und III (Fig. 19) scheidenden Platinplatte angesehen werden. Klar ist, daß wenn diese Platte nicht vorhanden wäre, die Batterie aus zwei Plattenpaaren und zwei Zellen bestände, und die günstigste Beschaffenheit zur Erzeugung [244] eines Stroms besäße. Die bei eingeschaltete Platinplatte, an deren einen Seite Sauerstoff und an deren anderen Seite Wasserstoff entwickelt wird (d. h. wenn der zersetzende Strom übergeht) kann als die Ursache eines Hindernisses betrachtet werden, das aus der Zersetzung des Wassers durch den elektrischen Strom entspringt, und ich habe sie daher gewöhnlich die Zwischenplatte (interposed plate) genannt.
1010) Um die Umstände zu vereinfachen, wurde anfangs in allen Zellen verdünnte Schwefelsäure, und als Zwischenplatten Platin angewandt, denn dann ist die anfängliche Intensität des Stroms, der sich zu bilden sucht, constant, indem er von der Kraft herrührt, mit welcher das Zink das Wasser zersetzt, und die widerstrebende Kraft der Zersetzung ist ebenfalls constant, da die Bestandtheile des Wassers bei ihrer Trennung an den Zwischenplatten durch keine Verwandtschaft oder durch keine aus der Natur der Platte oder der umgebenden Flüssigkeit entspringenden Action an den Elektroden (744) unterstützt werden.
1011) Als nur eine einfache Zink-Platin-Kette angewandt war, wurde der Strom durch Dazwischensetzung einer einzigen Platinplatte (Fig. 20) für alle practischen Entzwecke gänzlich gehemmt; wenigstens zersetzte er kein Wasser mehr. Dieß stimmt vollkommen mit den zuvor gegebenen Ansichten (910. 917. 973). Denn da das ganze Resultat abhängt von dem Kampf (opposition) der Kräfte an den Orten der Elektricitätserregung und der Elektrozersetzung, und da an beiden Orten Wasser zersetzt werden muß, so läßt sich nicht erwarten, daß das Zink eine so mächtige Anziehung zum Sauerstoff habe, um denselben nicht bloß dem mit ihm verbundenen Wasserstoff zu entreißen, sondern auch noch so viel Uebergewicht zu behalten, daß der Strom, nachdem er zu den zweiten Zersetzungsort übergegangen, daselbst im Stande sey, noch eine zweite Trennung der Bestandtheile des [245] Wassers zu bewirken. Solch ein Vorgang würde erfordern, daß die Anziehungskraft zwischen Zink und Sauerstoff unter diesen Umständen wenigstens doppelt so groß wäre als die Anziehungskraft zwischen dem Sauerstoff und Wasserstoff.
1012) Als zwei erregende Plattenpaare von Zink und Platin angewandt wurden, ward der Strom ebenfalls durch eine dazwischen gestellte Platinplatte für die Praxis gehemmt (Fig. 21). Anfangs war zwar eine sehr schwache Wirkung da, aber fast sogleich hörte sie auf. Ich werde von ihr und mehren ähnlichen Effecten späterhin (1017) reden.
1013) Drei Plattenpaare von Zink und Platin (Fig. 22) waren im Stande mit ihrem Strom eine eingeschaltete Platinplatte zu durchdringen und die Elektrolysirung des Wassers in der Zelle IV zu bewirken. Der Strom zeigte sich sowohl durch die fortdauernde Ablenkung des Galvanometers als durch die Blasen von Sauerstoff und Wasserstoff an den Elektroden in der Zelle IV. Also ist der angesammelte Kraftüberschuß dieser Zinkplatten, welche zur Zersetzung des Wassers thätig sind, zusammen genommen mehr als gleich der Kraft, mit welcher Sauerstoff und Wasserstoff zu Wasser verbunden sind, und er ist hinreichend die Trennung dieser Bestandtheile zu bewirken.
1014) Den drei Plattenpaaren von Zink und Platin wurden nun zwei Zwischenplatten von Platin entgegengesetzt, Fig. 23. Jetzt war der Strom gehemmt.
1015) Vier Plattenpaare von Zink und Platin wurden durch zwei dazwischengesetzte Platinplatten neutralisirt. Fig. 24.
1016) Fünf Paare Zink und Platin mit zwei Zwischenplatten von Platin (Fig. 25) gaben einen schwachen Strom; es fand eine bleibende Ablenkung des Galvanometers, und in den Zellen VI und VII eine Zersetzung statt. Allein der Strom war sehr schwach, sehr viel [246] schwächer als wenn alle dazwischen befindlichen Platten fortgenommen und bloß die beiden äußeren beibehalten wurden; denn wenn sie sechs Zoll aus einander in Eine Zelle gestellt wurden, gaben sie einen kräftigen Strom. Fünf erregende Plattenpaare mit zwei dazwischengesetzten Hemmplatten gaben also einen Strom, gar nicht vergleichbar mit dem eines einzigen ungehemmten Plattenpaars.
1017) Ich habe bereits gesagt, daß ein sehr schwacher Strom überging, wenn die Kette zwei Plattenpaare von Zink und Platin und eine Zwischenplatte enthielt (1012). Ein ähnlicher schwacher Strom ging jedesmal über, und selbst wenn nur Ein erregendes Plattenpaar mit vier Zwischenplatten von Platin angewandt wurde (Fig. 26) ließ sich bei ein Strom wahrnehmen, sowohl durch chemische Action auf eine Lösung von Jodkalium als auch durch das Galvanometer. Dieser Strom, glaube ich, rührt her von Elektricität, die bis unter die zur Zersetzung des Wassers erforderliche Intensität geschwächt worden ist (970. 984); denn Wasser kann eine Elektricität von so geringer Intensität vermöge einer ähnlichen Kraft leiten, wie sie die Metalle und die Kohle besitzen, wiewohl dasselbe eine Elektricität von höherer Intensität nicht ohne Zersetzung zu leiten vermag und ihr dann einen daraus erfolgenden Widerstand entgegensetzt. Bei einem elektrischen Strom unterhalb dieser Intensität wird wahrscheinlich eine Vermehrung der Anzahl der zwischengesetzten Platinplatten die Schwierigkeit der Leitung nicht erhöhen.
1018) Um eine Vorstellung von der mit Zusatz jeder Platinplatte[WS 1] steigenden Hemmkraft zu erhalten, wurden sechs voltasche Plattenpaare und vier Zwischenplatten von Platin, wie in Fig. 27, zusammengestellt. Es ging dann ein sehr schwacher Strom über (985. 1017). Wenn man eine der Zwischenplatten fortnahm, also nur drei beibehielt, ging ein etwas stärkerer Strom über. [247] Mit zwei Zwischenplatten wurde ein noch stärkerer Strom erhalten, und mit einer einzigen ein recht starker. Indeß war die Wirkung dieser Platten, genommen nach der Ordnung ihrer Dazwischensetzung, sehr ungleich, wie zu erwarten stand; denn die erste verzögerte den Strom mehr als die zweite, die zweite mehr als die dritte etc.
1019) Bei diesen Versuchen wurde sowohl amalgamirtes als nicht amalgamirtes Zink angewandt, allein im Allgemeinen mit gleichem Erfolg.
1020) Die eben beschriebenen Verzögerungs-Effecte wurden gänzlich geändert, wenn mit der Natur der Flüssigkeit zwischen den Platten eine Veränderung vorgenommen wurde, sey es in den sogenannten Erregungs- oder in den Verzögerungs-Zellen. Wenn man z. B. die erregende Kraft ungehindert ließ, nämlich nach wie vor reine verdünnte Schwefelsäure in den Erregungszellen anwandte, aber zu der Flüssigkeit in den Verzögerungszellen etwas Salpetersäure hinzusetzte, so wurde der Durchgang des Stroms sehr viel erleichtert. Wenn z. B. in dem Versuch mit Einem erregenden Plattenpaare und Einer Zwischenplatte (1011), Fig. 20, einige Tropfen Salpetersäure zu dem Inhalt der Zelle II hinzugesetzt wurden, ging der elektrische Strom mit bedeutender Stärke über (wiewohl er aus anderen Ursachen (1036. 1040) bald abnahm) und denselben guten Erfolg bewirkte die Salpetersäure bei Anwendung mehrer Zwischenplatten.
1021) Dieß scheint eine Folge davon zu seyn, daß die Schwierigkeit der Zersetzung des Wassers vermindert ist, wenn dessen Wasserstoff, statt frei ausgetrieben werden zu müssen, auf den Sauerstoff der Salpetersäure zur Bildung eines secundären Products an der Kathode übertragen werden kann, wie hier (752). Denn gemäß den schon (913) ausgesprochenen Ansichten von dem elektrischen Strom und dessen Wirkung widersteht das Wasser nun nicht mehr der Zersetzung mit dem vollen Betrag [248] der aus der gegenseitigen Anziehung seines Sauerstoffs und Wasserstoffs entspringenden Kraft, sondern diese Kraft ist theilweis aufgewogen, und folglich geschwächt durch die Anziehung des Wasserstoffs an der Kathode zu dem Sauerstoff der Salpetersäure daselbst, mit welchem es sich zuletzt verbindet, statt frei zu entweichen.
1022) Als ein wenig Salpetersäure in die erregenden Zellen gethan wurde, wurde der Durchgang des Stroms wiederum befördert, denn durch diesen Zusatz (906) wurde die Intensität des Stroms selbst erhöht. Als daher zugleich in die Erregungs- und in die Verzögerungs-Zellen[WS 2] etwas Salpetersäure geschüttet wurde, ging der Strom mit sehr beträchtlicher Stärke über.
1023) Bei Anwendung von verdünnter Salzsäure wurde ein Strom erzeugt und durchgelassen, der zwar den von der Schwefelsäure übertraf, dem von der Salpetersäure aber nicht gleich kam. Da die Salzsäure sich leichter zu zersetzen scheint als das Wasser (765) und da die Verwandtschaft des Zinks zum Chlor sehr kräftig ist, so ließ sich erwarten, daß mit ihr ein stärkerer Strom als mit der verdünnten Schwefelsäure erhalten werde, und daß er auch leichter durchgehe, da die Zersetzung bei schwächerer Intensität eintritt (912).
1024) In Bezug auf die Wirkung dieser Zwischenplatten ist es nöthig zu bemerken, daß sie durchaus nicht von der Größe der Elektroden oder von deren gegenseitigen Entfernung in der Säure abhängt, es sey denn, daß wenn ein Strom übergehen kann, Veränderungen in ihnen den Uebergang desselben befördern oder verzögern. Denn wenn man den Versuch mit Einer Zwischenplatte und Einem erregenden Plattenpaar wiederholt (1011), Fig. 20, und statt der Zwischenplatte zuweilen einen bloßen Draht, zuweilen eine sehr große Platte anwendet (1008) und auch die Endplatten und dahin abändert, daß man sie zuweilen sehr groß, zuweilen [249] aber bloße Drähte nimmt, so sind doch die Resultate den bereits beschriebenen gleich.
1025) Zur Erläuterung des Einflusses der Entfernung (der Platten) wurde ein Versuch mit zwei erregenden Plattenpaaren und Einer Zwischenplatte so angestellt (1012), Fig. 21, daß der Abstand zwischen den Platten in der dritten Zelle von der Dicke eines Blattes Fließpapier bis zu sechs bis acht Zoll vergrößert werden konnte. Dennoch war der Erfolg in beiden Fällen derselbe; er war sichtbar nicht größer, wenn die Platten bloß durch Papier getrennt waren, als wenn sie weit aus einander standen. Der Hauptwiderstand gegen den Strom hängt also nicht von der Quantität des dazwischen kommenden elektrolytischen Leiters ab, sondern von der Beziehung seiner Elemente zu der Intensität des Stroms, oder zu der chemischen Natur der Elektroden und der umgebenden Flüssigkeiten.
1026) Wenn Schwefelsäure angewandt wurde, bewirkte eine Verstärkung derselben in einer der Zellen keine Veränderung in den Effecten. Sie bewirkte keine Verstärkung des Stroms in den Erregungszellen (908), und auch keinen leichteren Durchgang desselben durch die Zersetzungszellen. Allein wenn zu sehr schwacher Schwefelsäure ein Paar Tropfen Salpetersäure hinzugesetzt wurden, dann stellte sich der eine oder andere Effect ein; und wie in einem Falle, wie dieser, wo die Erregungs- oder Leitungs-Wirkung eine directe Beziehung zu der Säure selbst besitzt, zu erwarten stand, erhöhte eine Verstärkung der Salpetersäure auch deren Kräfte.
1027) Jetzt wurde die Natur der Zwischenplatte geändert, um ihren Einfluß auf die Erscheinungen kennen zu lernen; und zuerst wurde das Platin durch amalgamirtes Zink ersetzt. Bei Anwendung Eines erregenden Plattenpaars und Einer solchen Zwischenplatte (Fig. 28) trat ein Strom ein, anscheinend eben so stark, wie wenn [250] keine Zwischenplatte vorhanden gewesen wäre. Am Platin in der Zelle II und an der Seite des zweiten Zinks in der Zelle I entwickelte sich Wasserstoff; allein an der Seite des Zinks in der Zelle II und an dem Zink in der Zelle I erschien kein Gas.
1028) Als zwei amalgamirte Zinkplatten statt einer dazwischen gestellt wurden (Fig. 29 Taf. I) war der Strom zwar noch kräftig, aber doch schon geschwächt. Mit drei Zwischenplatten von diesem Zink (Fig. 30) fand eine noch beträchtlichere Verzögerung statt, wiewohl noch ein guter Elektricitätsstrom überging.
1029) In der Meinung, die Wirkungslosigkeit des Zinks auf die verdünnte Säure sey die Ursache der Verzögerung, indem sie es nöthig mache, daß jede Platte, um Wasser zu zersetzen, etwas durch einen elektrischen Strom unterstützt werde, vermuthete ich, daß Platten von unamalgamirtem Zink einer solchen Unterstützung nicht bedürfen, und dem Uebergang des Stroms kein solches Hinderniß in den Weg legen würden. Diese Erwartung verwirklichte sich vollkommen bei Anwendung von zwei oder drei unamalgamirten Platten. Der elektrische Strom ging so frei hindurch, wie wenn keine solchen Platten im Wege standen. Sie erzeugten keinen Widerstand, weil sie Wasser ohne den Strom zersetzen konnten, und der letztere brauchte nur einen Theil der Kräfte, die auch ohne ihn wirksam gewesen wären, Richtung zu geben.
1030) Nun wurden Zwischenplatten von Kupfer angewandt. Anfangs schienen sie keinen Widerstand zu veranlassen, allein nach wenigen Minuten hörte der Strom ganz auf. Dieß scheint davon herzurühren, daß die Flächen jenen besonderen Zustand annehmen (1040), vermöge dessen sie einen umgekehrten Strom zu erregen trachten. Denn wenn eine oder mehre dieser Platten umgekehrt werden, was sich mittelst des Tassenkranzes (Fig. 18) leicht bewerkstelligen ließ, wurde der Strom auf einige Augenblicke kräftig erneut, und hörte dann [251] abermals auf. Platten von Platin und Kupfer, mit verdünnter Schwefelsäure zu einer voltaschen Säule angeordnet, vermochten wegen dieser eigenthümlichen Gegenwirkung nicht länger als ein Paar Minuten zu wirken.
1031) Alle diese Verzögerungseffecte, die sich durch Zersetzungen an Flächen äußern, zu denen die ausgeschiedenen Elemente eine größere oder geringere oder gar keine Verwandtschaft haben, zeigen in allgemeiner, jedoch hübscher Weise die chemischen Beziehungen und den Ursprung des elektrischen Stroms, so wie den Balancirungszustand (balanced state) der Verwandtschaften an dem Erregungs- und Zersetzungsort. Auf diese Weise vermehren sie die Beweise zu Gunsten der Einerleiheit dieser beiden (Verwandtschaften). Denn sie beweisen den Antagonismus der chemischen Kräfte in dem elektromotorischen Theil zu den chemischen Kräften in dem eingeschalteten Theile; sie zeigen, daß der erstere elektrische Wirkungen erzeugt, und daß der letztere sich diesen widersetzt; sie bringen die beiden in directe Relation; sie thun dar, daß jeder von ihnen den andern bedingen kann, kehren anscheinend Ursache und Wirkung um, und beweisen, daß die chemische und elektrische Action nur zweierlei Aeußerungen eines einzigen Wesens oder einer einzigen Kraft darstellen (916 ff.).
1032) Da Wasser und andere Elektrolyte unzersetzt (986) die Elektricität zu leiten vermögen, sobald nur die Intensität der Elektricität schwach genug ist, so ist ganz klar, daß man nicht in allen Fällen mit voller Wahrheit sagen könne, die Elektricität erzeuge bei ihrem Durchgang durch einen Elektrolyt jedesmal einen festen Zersetzungseffect. Allein die Elektricitätsmenge, welche in einer gegebenen Zeit durch einen Elektrolyt gehen kann, ohne eine Zersetzung zu bewirken, ist so klein, daß sie mit der zu einer mäßigen Zersetzung erforderlichen keinen Vergleich aushält. Und bei einer Elektricität von größerer als der zur Zersetzung erforderlichen Intensität [252] habe ich bis jetzt noch keine merkliche Abweichung von dem in der siebenten Reihe dieser Untersuchungen (783. etc.) entwickelten Gesetz der festen elektrolytischen Action aufgefunden.
1033) Ich kann diesen Abschnitt nicht verlassen, ohne nicht noch der wichtigen Versuche des Hrn. A. De La Rive über die Wirkung der Zwischenplatten Erwähnung zu thun[19]. Da ich zu der Annahme geführt worden bin, daß dergleichen nur in sofern dem Durchgang des elektrischen Stroms einen Widerstand entgegensetzen als sie zu neuen Zersetzungen Anlaß geben, so hatte ich nicht nöthig, die von jenem Physiker beschriebenen besonderen Effecte in Betracht zu ziehen, und ich bin um so mehr geneigt davon abzustehen, als ich zugleich in die Ansichten von Sir Humphry Davy[20] über denselben Gegenstand, und auch in die damit verknüpften von Marianini[21] und Ritter[22] hätte eingehen müssen.
1034) Wenn eine gewöhnliche voltasche Batterie in Thätigkeit gesetzt wird, so bringt ihre eigne Thätigkeit gewisse Effecte hervor, welche auf sie rückwirken und eine bedeutende Schwächung ihrer Kraft veranlassen. Dadurch wird sie in Bezug auf die Quantität des Effects, welchen sie hervorzubringen fähig ist, ein sehr wandelbares Instrument. Zum Theil sind diese Erscheinungen schon bekannt und verstanden; allein da ihre und anderer damit zusammentreffender Resultate Wichtigkeit deutlicher werden wird [253] durch Beziehung auf die schon angegebenen Grundsätze und Erfahrungen, so habe ich es für nützlich gehalten ihrer hier kurz zu erwähnen.
1035) Wenn die Batterie in Thätigkeit ist, bewirkt sie, daß solche Substanzen gebildet und mit den Platten in Berührung gestellt werden, welche ihre Kraft sehr schwächen oder gar einen Gegenstrom zu erzeugen trachten. Sir Humphry Davy[23] hält sie für hinreichend, die Erscheinungen an Ritter’s secundären Säulen, so wie die von Hrn. A. De La Rive beobachteten Wirkungen der Zwischenplatten zu erklären.
1036) Ich habe bereits bemerkt, daß die Kraft des Stroms dadurch in einigen Fällen bis auf ein Achtel oder Zehntel ihrer anfänglichen Stärke zurückgeführt werden kann, und habe Beispiele angeführt, wo die Störung sehr grob war. Bei einem Versuche, wo Ein voltasches Paar und eine Zwischenplatte von Platin mit verdünnter Schwefelsäure in den Zellen (Fig. 31) angewandt ward, wurden die Verbindungsdrähte so geordnet, daß das Ende des Drahts 3 nach Belieben auf ein mit Jodkalium-Lösung befeuchtetes Papier oder geradezu auf die Platinplatte daselbst gesetzt werden konnte. Wenn nach einiger Zeit, während welcher die Kette nicht geschlossen worden war, der Draht 3 auf das Papier gesetzt wurde, ergaben sich Anzeigen von einem Strome, eine Zersetzung trat ein und das Galvanometer wich ab. Ließ ich den Draht 3 das Metall bei berühren, so ward ein verhältnißmäßig starker plötzlicher Strom erzeugt, der das Galvanometer ergriff; aber er hielt nur einen Augenblick an, die galvanometrische Wirkung hörte auf, und wenn nun der Draht 3 auf das Papier bei gesetzt wurde, traten keine Anzeigen von einer Zersetzung auf. Nach Aufhebung des Drahts und gänzlicher Unterbrechung des Stroms für eine Weile nahm der Apparat wiederum seine anfängliche Stärke an, erforderte jedoch dazu [254] fünf bis zehn Minuten; und wenn dann, wie zuvor, der Contact zwischen 3 und hergestellt wurde, erschien wiederum ein momentaner Strom und gleich darauf hörten anscheinend alle Effecte auf.
1037) Zuletzt war ich im Stande diese Wirkung dem Zustande der die Zinkplatte in der Zelle I berührenden Flüssigkeitsschicht zuzuschreiben. Die Säure dieser Schicht wird augenblicklich durch das gebildete Oxyd neutralisirt; die Oxydation des Zinks kann demnach nicht mit der früheren Leichtigkeit vor sich gehen; und da so die chemische Action unterbrochen ist, wird mit ihr auch die voltasche Action geschwächt. Die Ruhezeit wird erfordert, damit diese Flüssigkeitsschicht verbreitet und durch andere Säure ersetzt werden konnte. Aus dem bedeutenden Einfluß dieser Ursache bei Versuchen mit einfachen Plattenpaaren von verschiedenen Metallen, mit denen ich einmal beschäftigt war, und aus der ungemeinen Sorgfalt, die zur Vermeidung desselben erforderlich war, kann ich nicht umhin, den Verdacht zu hegen, und die Experimentatoren darauf aufmerksam zu machen, daß er häufiger, als sie es denken, störend einwirkt.
1038) Wenn man die Wirkung dieser Quelle der unregelmäßigen Wirkung des voltaschen Apparats bei zarten Versuchen erwägt, muß erinnert werden, daß es nur die sehr kleine, direct mit dem oxydirbaren Metall in Berührung stehende Portion der Flüssigkeit ist, welche in Bezug auf die Veränderung ihrer Natur betrachtet zu werden braucht; und diese Portion wird nicht leicht aus ihrer Lage an der Oberfläche des Metalls (582. 605) verdrängt, besonders wenn dieß Metall eine rauhe unregelmäßige Oberfläche hat. Zur Erläuterung dieses will ich einen merkwürdigen Versuch anführen. Eine polirte Platinplatte (569) wurde nur auf einen Augenblick in heiße concentrirte Schwefelsäure getaucht, dann in destillirtes Wasser, darin herumgeführt, herausgenommen [255] und trocken gewischt; darauf wurde sie in eine zweite Portion destillirten Wassers getaucht, darin herumbewegt und abermals trocken gewischt; jetzt ward sie in eine dritte Portion destillirten Wassers getaucht, darin beinahe acht Secunden herumbewegt, und nun, ohne Abwischen, in eine vierte Portion destillirten Wassers gebracht und fünf Minuten darin gelassen. Die beiden letzten Portionen Wasser wurden dann auf Schwefelsäure geprüft; die dritte zeigte keine merkbaren Spuren von dieser Säure, aber die vierte gab nicht nur sichtbare, sondern auch für die Umstände reichliche Anzeigen von derselben. Dieß Resultat zeigt genugsam, mit welcher Schwierigkeit die das Metall berührende Portion einer Flüssigkeit dasselbe verläßt; und da in der voltaschen Kette die Berührung zwischen der Flüssigkeit und dem Metall so innig und vollkommen wie möglich seyn muß, so ist leicht einzusehen, wie schnell und stark er sich durch die Masse der Flüssigkeit in der Zelle verändere und wie schwächend er auf die Kraft der Batterie einwirken muß.
1039) In der gewöhnlichen voltaschen Säule kommt der Einfluß dieses Effects in allen Stärkegraden vor. Die Enden eines Trogs von zwanzig Wollaston’schen Plattenpaaren wurden mit dem Volta-Elektrometer, Fig. 11 (Taf. III Bd. XXXIII), der siebenten Reihe dieser Untersuchungen (711) verbunden, und nach fünf Minuten die Anzahl der Gasblasen, die in Folge der Wasserzersetzung von dem Ende der Röhre aufstiegen, aufgezeichnet. Ohne die Platten zu bewegen, wurde die Säure zwischen dem Kupfer und Zink mit einer Federfahne umgerührt. Sogleich entwickelten sich die Gasblasen rascher, fast doppelt so schnell wie vorher. Sehr einleuchtend ist, daß das Umrühren mit der Feder ein sehr unvollkommenes Mittel war, die Säure an den Platten, in der Zelle auf ihren anfänglichen gleichmäßigen Zustand zurückzuführen, und dennoch wurde dadurch die [256] Kraft der Batterie mehr als verdoppelt. Die anfängliche Wirksamkeit einer Batterie, die bekanntlich höher ist als die später anhaltende, ist fast gänzlich Folge des günstigen Zustandes, in welchem sich die mit den Platten in Berührung stehende Säure befindet.
1040) Eine zweite Ursache zur Schwächung der voltaschen Batterie, entspringend aus ihrer eigenen Thätigkeit, liegt in dem ungewöhnlichen Zustand der Metall-Oberfläche, welcher, glaube ich, von Ritter[24] zuerst beschrieben und als das Wirkende seiner secundären Säulen bezeichnet, auch späterhin von Marianini und A. De La Rive so wohl untersucht ist. Unterhält man den Apparat Fig. 31 (1036) eine oder zwei Stunden lang in Thätigkeit, den Draht 3 dabei auf die Platte gestellt, um den Strom einen freien Durchgang zu gestatten, und unterbricht darauf den Contact auf zehn oder zwölf Minuten, so wird doch bei seiner Wiederherstellung nur ein schwacher Strom übergehen, bei weitem kein so starker als man wohl erwartet hätte. Wenn man ferner und durch einen Metalldraht verbindet, geht von durch die Säure nach ein momentaner Strom über, also in umgekehrter Richtung mit dem, welchen die Wirkung des Zinks in dieser Vorrichtung erzeugt. Und nachdem dieß geschehen ist, vermag der Hauptstrom wieder, wie anfangs, durch das ganze System zu gehen, allein durch seinen Uebergang versetzt er wieder die Platten und in den früheren entgegenstrebenden Zustand. Dieß ist im Allgemeinen die von Ritter, Marianini und De La Rive beschriebene Erscheinung. Sie leistet der Wirkung einer Säule einen sehr großen Widerstand, besonders wenn diese aus einer kleinen Anzahl von Plattenpaaren besteht und ihr Strom durch viele Zwischenplatten gehen muß. Der Widerstand ist verschieden nach der Flüssigkeit, in welche [257] die Zwischenplatten eingetaucht sind, nach der Stärke der Säule, nach der Zeit der Wirkung, und besonders nach zufälligen Entladungen der Säule durch unachtsames Berühren oder Umkehren der Platten während der Versuche. Auf alle diese Umstände muß man sorgfältig achten, wenn man die Entstehung, Stärke und Veränderung des voltaschen Stroms untersuchen will. Ihren Einfluß vermied ich in den bereits (1036) beschriebenen Versuchen dadurch, daß, ehe ich die von dem Zustand der die Zinkplatte berührenden Flüssigkeit abhängige Wirkung beobachtete, die Platten und in Berührung setzte, so wie auch durch andere Vorsichtsmaßregeln.
1041) Bei Verknüpfung eines Apparats von mehren Platinplatten, wie der Fig. 26 (1017), mit einer Batterie, die einen Strom durchzutreiben vermochte, erhielt sie die zur Hervorbringung eines Gegenstroms erforderliche Kraft in sehr beträchtlichem Grade.
1042) Schwache und matte Entladungen dürfen niemals gleichzeitig mit starken und frischen in verschiedenen Zellen eines Troges oder in verschiedenen Trögen einer Batterie angewandt werden. In allen Zellen muß die Flüssigkeit gleich seyn; sonst unterstützen die Platten in den schwächeren Zellen nicht die in den stärkeren Zellen erzeugte und durch sie durchgelassene Elektricität, sondern verzögern ihren Durchgang. Jede so beschaffene Zinkplatte muß in der Zersetzungskraft unterstützt werden, ehe der Gesammtstrom zwischen ihr und der Flüssigkeit übergehen kann. Wenn z. B. in einer Batterie von funfzig Plattenpaaren zehn der Zellen eine schwächere Ladung erhalten als die übrigen, so ist es eben so, wie wenn zehn Zersetzungsplatten dem Uebergang des Stroms von vierzig erzeugenden Plattenpaaren entgegengestellt würden (1031). Hieraus der namhafte Kraftverlust, und dieß der Grund, warum, wenn die zehn Plattenpaare fortgenommen werden, die übrigbleibenden vierzig Paare stärker wirken als alle funfzig.
[258] 1043) Fünf solcher Tröge, jeder von zehn Plattenpaaren, wurden vorgerichtet, vier von ihnen mit einer guten gleichmäßigen Ladung von Säure, und die fünfte mit der theilweis neutralisirten Säure einer gebrauchten Batterie. Nachdem sie richtig geordnet und mit einem Volta-Elektrometer (711) verbunden worden, lieferten die sämmtlichen fünfzig Plattenpaare 1,1 Kubikzoll Sauerstoff und Wasser in einer Minute. Als aber einer der Verbindungsdrähte fortgenommen wurde, so daß nur vier Tröge die Batterie ausmachten, erzeugten diese mit demselben Volta-Elektrometer und in derselben Zeit 8,4 Kubikzoll Gas. Fast sieben Achtel von der Kraft der vier Tröge war also durch deren Verknüpfung mit dem fünften Trog verloren gegangen.
1044) Nach diesem Gebrauche wurde dieselbe Batterie mit einem Volta-Elektrometer (711) so verbunden, daß durch ein rasches Wechseln der Verbindungsdrähte der Strom der ganzen Batterie oder eines Theils von ihr nach einander eine gegebene Zeit lang durch das Instrument geleitet werden konnte. Die ganze Batterie entwickelte in einer halben Minute 0,9 Kubikzoll Sauerstoff und Wasserstoff; die vierzig Platten entwickelten in derselben Zeit 4,6 Kubikzoll. Darauf entwickelten in einer halben Minute die sämmtlichen Platten 1,0 Kubikz., dann die zehn schwach geladenen 0,4 Kubikz., und endlich wieder die sämmtlichen: 1,5 Kubikzoll. Diese Resultate zeigen genugsam den schädlichen Einfluß der Verknüpfung starker und schwacher Ladungen zu Einer Batterie[25].
1045) Aus ähnlichem Grunde muß die Verknüpfung von starken und schwachen Plattenpaaren sorgfältig vermieden werden. Ein Plattenpaar von Kupfer und Platin [259] mit einem Plattenpaar von Zink und Platin übereinstimmend in verdünnte Schwefelsäure getaucht, hemmte die Wirkung des letzteren, und selbst zwei solcher Paare, fast eben so stark als eine Zwischenplatte von Platin (1011), oder wie wenn das Kupfer selbst Platin gewesen wäre. In der That wurde es eine zersetzende Zwischenplatte, und deshalb mit dem Platin, statt eines unterstützenden, ein verzögerndes Paar.
1046) Eine Umkehrung der Platten in der Batterie, zufällig oder nicht, hat einen ungemein schädlichen Einfluß. Nicht bloß, daß die umgekehrten Platten einen Gegenstrom zu erzeugen vermögen, sondern auch sie wirken hemmend als indifferente Platten, und verlangen an ihrer Oberfläche die Vollziehung einer Zersetzung übereinstimmend mit dem Lauf des Stroms, ehe dieser übergehen kann. Sie widersetzen sich also dem Strom zunächst, wie es Platin als Zwischenplatten thun würde (1011 bis 1018), und fügen eine Widerstandskraft als voltasche Gegenplatten hinzu. Ich finde, daß wenn man in einer Reihe von vier Plattenpaaren aus Zink und Platin in verdünnter Schwefelsäure eins derselben umgekehrt, dadurch fast die Kraft des Ganzen aufgehoben wird.
1047) Es giebt noch manche andere Ursachen zur Rückwirkung, Verzögerung und Unregelmäßigkeit in der voltaschen Batterie. Unter ihnen ist die nicht ungewöhnlichste die Fällung des Kupfers auf das Zink in der Zelle, auf deren Schädlichkeit bereits früher (1006) aufmerksam gemacht wurde. Ihr Interesse ist indeß wohl nicht groß genug, um eine weitere Verlängerung dieser mehr auf die Theorie als auf die practische Anwendung der voltaschen Säule gerichteten Abhandlung zu rechtfertigen.
Zusatz. – Viele der Ansichten und Versuche in dieser Reihe meiner Experimental-Untersuchungen berichtigen und erweitern, wie man sehen wird, die Theorie der elektro-chemischen Zersetzung, welche ich in der fünften und siebenten Reihe gegeben habe. Die Ausdrücke, [260] welche ich jetzt ändern würde, sind die in Bezug auf die Unabhängigkeit der entwickelten Elemente zu den Polen oder Elektroden und die Beziehung ihrer Entwicklung zu gänzlich inneren Kräften (524. 537. 661). Die gegenwärtige Abhandlung zeigt meine Ansichten vollständig, und ich verweise dieserhalb auf die Paragraphen 891. 904. 910. 917. 918. 947. 963. 1007. 1031 u. s. w. Ich hoffe, dieser Zusatz möge vor der Hand als Berichtigung für hinlänglich erachtet werden. Eine Revision der ganzen Theorie von der elektro-chemischen Zersetzung möchte ich lieber aufschieben, bis ich klarer einsehe, wie die in Rede stehende Kraft manchmal als verbunden mit Körpertheilchen und ihnen chemische Anziehung gebend, manchmal dagegen als freie Elektricität zu erscheinen vermag (433. 957)[26].
Royal Institution. – 31. März 1834.
- ↑ That the clorid stands first u. s. w.
- ↑ Wollaston, Philosoph. Transact. 1801, p. 427.
- ↑ Ich will nicht behaupten, daß in solchen Fällen gar keine Spuren von Elektricität erscheinen. Ich meine nur, daß auf keine Weise Elektricität erregt werde, die von den die voltasche Elektricität erregenden Ursachen herrührte, oder zu ihnen Bezug hätte, [21] oder ihnen proportional wäre. Die zuweilen auftretende Elektricität ist der kleinst mögliche Bruch von der, welche die thätige Substanz erzeugen kann, wenn sie zu einer voltaschen Wirkung vorgerichtet wird; wahrscheinlich ist sie von dieser nicht 1/100000, selbst nicht 1/1000000, und sehr wahrscheinlich stammt sie aus einer ganz anderen Quelle her.
- ↑ Man sieht, dieß stimmt mit Humphry Davy, welcher experimentell zu der Ansicht gelangte, daß Säuren und Alkalien bei ihrer Verbindung keinen elektrischen Strom hervorrufen. Philosoph. Transact. f. 1826, p. 398.
- ↑ Es versteht sich, glaube ich, von selbst, daß ich hier nicht behaupte, jede kleine, zufällige und bloß mögliche Wirkung, die während der chemischen Action aus unbedeutenden Störungen des elektrischen Fluidums entspringen kann, in Rechnung zu ziehen, sondern bloß suche die Actionen, von denen die Kraft der voltaschen Batterie wesentlich abhängt, zu unterscheiden und zu identificiren.
- ↑ Elements of chemical Philosophy, p. 149, oder Phil. Transact. 1826, p. 403.
- ↑ Elements of chemical Philosoph, p. 148.
- ↑ Gebraucht man Salpeter-Schwefelsäure, so ist der Funke kräftiger; allein es können dann locale chemische Actionen eintreten, die, ohne den Metallcontact zu erfordern, fortdauern.
- ↑ Es ist allgemein angenommen worden, daß bei Schließung einer einfachen Kette kein Funken entstehe; allein die bereits in diesem Aufsatz aufgestellten Beobachtungen führten mich darauf, einen solchen zu erwarten. Der Verbindungsdraht muß indeß kurz seyn; denn bei Anwendung eines langen Drahts treten Umstände ein, die einen großen Einfluß auf den Funken ausüben.
- ↑ Philosoph. Transact. 1807.
- ↑ Ibid. 1826, p. 383.
- ↑ Ibid. 1826, p. 389.
- ↑ Ich beabsichtigte früher in einer Anmerkung sämmtliche Aufsätze derjenigen Physiker aufzuführen, welche den Ursprung der Elektricität in der voltaschen Säule von dem Contact oder von der chemischen Action oder von beiden Ursachen ableiten; allein nach dem Erscheinen des ersten Theils von Hrn. Becquerel’s wichtigem und werthvollem Traité de l’Electricité et du Magnétisme hielt ich es für besser, hinsichtlich dieser Citate und der von jenen Physikern aufgestellten Ansichten, auf dieses Werk zu verweisen. Man sehe S. 86, 91, 104, 110, 112, 117, 118, 120, 151, 152, 224, 227, 228, 232, 233, 252, 255, 257, 258, 290 u. s. w. – 3. Juli 1834.
- ↑ Diese Annalen, Bd. XXXI S. 237. 238 und 244.P.
- ↑ Biblioth. universelle, T. 43 p. 341 (Annal. Bd. XIX S. 221).
- ↑ Jameson’s Edinburgh Journ. Oct. 1828.
- ↑ Hr. Sturgeon ist natürlich unbekannt mit der festen Elektricitätserzeugung durch chemische Action, und führt in der That den Versuch als den strengsten Beweis gegen die chemische Theorie des Galvanismus an.
- ↑ Phil. Transact. 1826. p. 405.
- ↑ Annales de chim. et de phys. T. XXVIII p. 190 (dies. Ann. Bd. XV S. 98 und 122.).
- ↑ Philos. Transact. 1826, p. 413.
- ↑ Annal. de chim. et de phys. T. XXXIII p. 117. 119.
- ↑ Journ. de phys. T. LVII p. 349. 350.
- ↑ Philosoph. Transact. 1826, p. 413.
- ↑ Journal de physique, T. LVII p. 349.
- ↑ Die allmälige Zunahme der Wirkung sämmtlicher funfzig Plattenpaare rührte davon her, daß bei dem Durchgang des Stroms durch den schwach geladenen Trog die Temperatur und damit auch die erregende Kraft der Flüssigkeit daselbst erhöht werde.
- ↑ Im Januarheft der Annales de chimie et de physique von diesem Jahre befindet sich ein kurzer Aufsatz von Hrn. Matteucci in Florenz, welchen Alle die, welche den wichtigen Untersuchungen des Hrn. Faraday gefolgt sind, nicht ohne Befremden werden lesen können, indem sie darin den Verfasser mit nichts Geringerem als der Entdeckung der festen elektrolytischen Action auftreten sehen, in ähnlicher, aber mangelhafterer Weise nachgewiesen, wie es von dem englischen Physiker geschehen ist. Hrn. Matteucci’s Aufsatz datirt vom October 1834, Hrn. Faraday’s siebente Abhandlung dagegen vom 1. Dec. 1833, ja dessen vierte Abhandlung, worin das nämliche Gesetz bereits ganz deutlich ausgesprochen ist, gar schon vom 15. April desselben Jahres. Wem von beiden hier also die Ehre der Priorität gebühre, liegt klar am Tage. Möglich, wenngleich nicht sehr wahrscheinlich, daß die Arbeiten des Auslandes so spät zur Kenntniß der Florentiner Physiker gelangen (man erinnere sich nur, wie schnell ihnen die Kunde von der Magneto-Elektricität zugekommen ist); – wie aber in Paris die Entdeckung Faraday’s so unbekannt seyn (oder ignorirt werden) kann, daß daselbst ein Jahr hernach der Aufsatz des Hrn. Matteucci ohne irgend eine Bemerkung in’s Publicum gebracht wird, ist in der That unbegreiflich. Der Wissenschaft freilich gilt es gleich, durch wen sie erweitert wird (wiewohl Keiner diesen Satz anerkennt, sobald er selbst dabei betheiligt ist); – aber eine so wichtige Entdeckung, wie die letztere des Hrn. Faraday, unstreitig der einzige wahre Fortschritt in unserer Kenntniß von der chemischen Wirksamkeit der Elektricität seit dem Jahre 1800, dem Jahre der Entdeckung der Wasserzersetzung durch die Säule, – eine solche Entdeckung fordert doch wohl zu einigem Dank gegen ihren Urheber auf, und die öffentliche Anerkennung seiner wohl begründeten Prioritätsrechte ist sicher der geringste Dank, den man ihm bringen kann.P.